Bases morfológicas de la implantación dental.
Traducción automática
El artículo original está escrito en idioma RU (enlace para leerlo) .
La implantación dental es una tecnología moderna que permite implantar una raíz artificial en el tejido óseo de la mandíbula del paciente. El diseño del implante consta de un tornillo y un pilar de titanio. Posteriormente, los implantes se utilizan como soporte de estructuras ortopédicas. El pilar se instala dentro del tornillo de titanio sólo después de que éste haya cicatrizado.
La colocación del implante se acompaña de un traumatismo en el tejido óseo del paciente, luego se inician los procesos de regeneración, que conducen a la formación de tejido óseo primero reticulofibroso y posteriormente laminar.
Obtenga más información sobre los factores que influyen en la cicatrización del implante en el seminario web Implantación en una sola etapa con carga inmediata .
Clínicamente, la regeneración ósea normal debería conducir a un contacto directo y estrecho entre el tejido óseo y el implante; en otras palabras, la curación del implante equivale a la osteointegración.
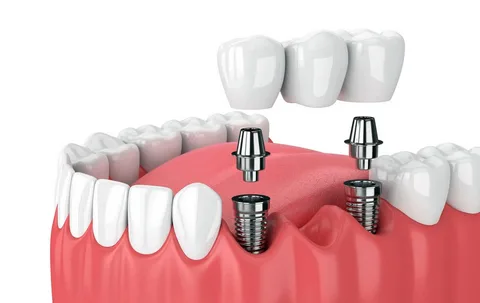
Figura 1. Implantación dental.
Anteriormente se creía que el tejido fibroso que lo rodea desempeña un papel importante en la osteointegración del implante. Los científicos supusieron que las fibras de colágeno comienzan a crecer gradualmente en él, por lo que el implante está conectado al hueso a través de tejido fibroso, de manera similar a las fibras de Sharpey.
El uso de diseños planos de implantes Linkow y Weiss se basa en una implantación fibrosa. En este sentido, su superficie estaba dotada de irregularidades, curvas y agujeros que permitían que el tejido óseo creciera a través del implante.
Si el proceso de curación es desfavorable o si se aplica una carga prematura excesiva al implante, se forma una capa gruesa de tejido conectivo entre este y el hueso alveolar y se produce la desintegración. El tejido fibroso no puede considerarse un soporte fiable para un implante, el funcionamiento de este último con este soporte no supera los diez años.
El injerto de implantes Linkow y Weiss de forma plana se basa en otro mecanismo: la integración osteofibrosa, que se basa en el contacto directo parcial que se forma debido al crecimiento de tejido óseo en los orificios del implante. En este caso, la proporción de contacto directo con el tejido óseo debe ser del 22% del área del cuerpo del implante.
El tipo de integración está determinado por las cargas iniciales sobre el implante. Con la integración osteofibrosa, la capa de soporte tiene características de absorción de impactos debido a la cápsula fibrosa elástica. Los científicos no pudieron demostrar experimentalmente la formación de fibras entre el tejido fibroso del implante y la superficie del hueso. La curación exitosa de diseños de implantes planos ha sido poco estudiada. Además, algunas estructuras funcionan desde hace 25 años.
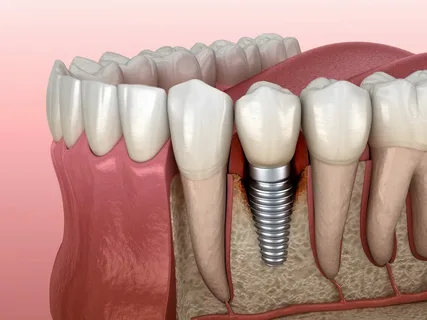
Figura 2. Osteointegración del implante.
Etapas de la curación ósea después de la implantación.
Una herida ósea después de un implante dental pasa por las mismas etapas de curación que son características de la curación de una herida debido a una fractura de mandíbula. Los patrones de curación dependen del material del implante y del tipo de procedimiento quirúrgico.
La curación de una herida ósea incluye las siguientes etapas:
inflamación,
proliferación,
cicatrización.
Etapa de inflamación
El inicio de la etapa de inflamación se asocia con una reacción a una interferencia extraña, la detección de un cuerpo extraño en los tejidos, así es como el cuerpo percibe el implante. La duración de la etapa de inflamación es de unos 10 días, pero su duración puede aumentar.
Modificación
Un implante colocado en un lecho óseo provoca alteración en la etapa de inflamación. Se considera alteración al conjunto de los siguientes cambios:
daño a los elementos celulares,
movilización de las defensas celulares,
activación de las defensas de todo el organismo en su conjunto.
Características generales de los procesos de alteración.
Un conjunto de cambios morfológicos y bioquímicos.
Reacciones vasculares locales.
Se observa necrosis tisular en el sitio de la lesión.
El cuerpo desencadena reacciones de sistemas reguladores integrales, donde las sustancias vasoactivas y quimiotácticas juegan un papel importante que determina el grado de inflamación.
Trastornos distróficos de las células y la sustancia intercelular.
Las proteínas se absorben en la superficie de los implantes.
En la superficie del implante, aumenta la agregación plaquetaria, aumenta la coagulación en cascada, se liberan citocinas y se activan reacciones celulares específicas e inespecíficas.
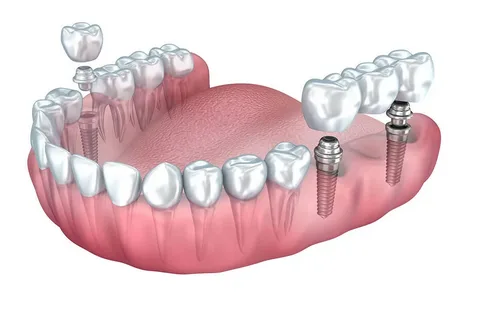
Figura 3. Rehabilitación bucal total mediante implantación.
Es difícil identificar signos tempranos de exudación y alteración, ya que durante la primera semana predominan los procesos reparativos. Las reacciones que se producen en los tejidos provocan la aparición de acidosis tisular y un aumento de la presión osmótica. En el borde del tejido óseo y el implante se acumulan productos que provocan alteraciones de la homeostasis y la permeabilidad vascular. El criterio principal para la transición de la etapa de alteración a la de exudación es una violación de la permeabilidad vascular.
Exudación
Características generales de los procesos de exudación.
La hemodinámica está alterada.
La hiperemia vascular arterial se desarrolla bajo la influencia de mediadores inflamatorios, se altera la salida de sangre y linfa. Un papel importante en la implementación de estos procesos pertenece a la histamina y la serotonina.
Se observa trombosis local.
Se observa acidosis, que conduce a un aumento de la hidrofilicidad de los coloides tisulares y, como consecuencia, de las fibras de colágeno, lo que contribuye a una ralentización del flujo sanguíneo en los vasos pequeños debido al debilitamiento de las paredes.
Una ralentización significativa del flujo sanguíneo puede provocar estasis.
Se activa el sistema del complemento.
La exudación y su consecuencia, el aumento del edema, desempeñan una función protectora, pero provocan un aumento de la presión arterial en los vasos pequeños y de la presión osmótica en los tejidos circundantes. El resultado es el movimiento de leucocitos hacia el área dañada. La migración de leucocitos siempre se dirige al área de daño tisular. Si el curso es favorable, al tercer día después de la operación de implantación, comienza a restablecerse la circulación sanguínea en los tejidos dañados.
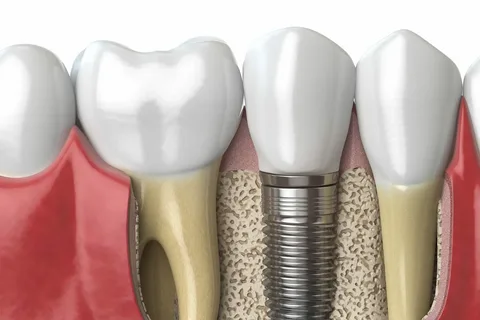
Figura 4. Contacto íntimo entre el hueso y la superficie del imantado.
Etapa de proliferación
En esta etapa, se observa diferenciación celular y el trofismo tisular se restablece gradualmente, lo que es evidencia de la curación de la herida ósea. La duración de esta etapa es de aproximadamente 6 semanas, pero los signos iniciales pueden aparecer ya al tercer día después de la cirugía.
En el tejido conectivo adyacente al implante se observan los siguientes procesos:
neoplasia de vasos sanguíneos,
proliferación y diferenciación celular,
activación de la síntesis de colágeno,
movimiento de elementos celulares al sitio de la inflamación.
Se produce epitelización de la herida, diferenciación celular, crecimiento y queratinización del epitelio. El desarrollo de anastomosis vasculares provoca la restauración de la microcirculación y un aumento de la saturación de oxígeno de los tejidos, lo que acelera el flujo de nutrientes.
En la etapa de proliferación ocurren los siguientes procesos reparativos:
Los elementos inmaduros del tejido conectivo se transforman en tejido de granulación joven.
se forma tejido cicatricial joven,
El tejido cicatricial se reconstruye gradualmente.
Etapa de regeneración
Los procesos de regeneración se observan desde los primeros días después de la implantación, alcanzan su máximo a finales de mes. Siempre que no se apliquen cargas al cuerpo del implante, comienza a formarse tejido óseo a su alrededor y se establece su suministro de sangre. El callo formado está representado por elementos fibrocartilaginosos, que es similar a la osificación endocondral.
El establecimiento del trofismo y el flujo de oxígeno al lugar del daño estimula la hemodinámica y la microcirculación locales, lo que tiene un efecto beneficioso sobre la reconstrucción del tejido óseo.
La mineralización ósea es causada por la carga sobre el implante. Sin carga, el tejido óseo que está en contacto directo con el implante tiene muchos espacios medulares, huecos en la sustancia esponjosa. Mientras que alrededor del implante cargado se determina tejido óseo densamente formado.
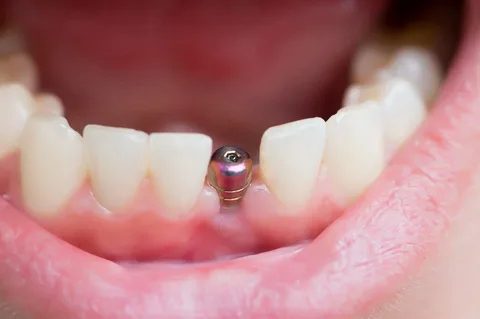
Figura 5. Vista en la cavidad bucal.
La citogénesis de células mesenquimales inmaduras y su posterior diferenciación conduce a la formación de una matriz compuesta de colágeno, glucosaminoglicanos, glicoproteínas y glicolípidos; esta matriz sufre una reestructuración. La futura matriz ósea inmadura se remodela en respuesta a la carga del implante, así como a la recesión ósea fisiológica. Estos mecanismos subyacen al proceso de curación del implante.
Si la curación es favorable, el implante está bien adaptado; en su superficie las células adventicias se diferencian y rellenan las zonas de hueso dañado. Al mismo tiempo, se observan procesos de reabsorción y osificación en el tejido óseo. La tasa de mineralización del hueso recién formado puede alcanzar 1 mm por día.
Todas las tecnologías, métodos y herramientas modernos para lograr un resultado estable del tratamiento con implantes se recopilan en el curso en línea Regeneración guiada e implantación de navegación .