In Vitro оценка эффективности остеогенной дифференцировки клеток в присутствии пластин для костной пластики челюстей из полилактида (PLA) с различным составом
Актуальность. Врачи-стоматологихирурги сталкиваются с необходимостью установки дентальных имплантатов для восстановления функций зубочелюстной системы у пациентов с костными дефектами разной этиологии. Одним из методов костной пластики челюстей для восстановления дефекта является применение титановых мембран, однако это подразумевает дополнительный этап — извлечение каркаса — перед проведением имплантации. Использование биорезорбируемых материалов для изготовления мембран может стать новым шагом в аугментации костной ткани челюстей, снизить риски послеоперационных осложнений и время работы хирурга.
Цель. Целью данного исследования было изучить влияние разных полимерных составов индивидуальных каркасов для костной пластики на процессы пролиферации и остеогенной дифференцировки в условиях in vitro.
Материалы и методы. В исследовании были подготовлены пластины размером 10 х 10 х 0,5 мм из чистого полилактида (PLA), полилактида с добавлением 15% масс. наночастиц гидроксиапатита (PLA/HA), сополимеров полилактида с гликолидом с соотношениями мономеров 60:40 и 85:15 (PLGA 60:40 и 85:15). Для оценки влияния экспериментальных образцов на процессы пролиферации и остеогенной дифференцировки клеток были использованы гингивальные фибробласты, которые культивировались в низкоглюкозной питательной среде, далее в лунки помещали образцы. Остеогенную дифференцировку индуцировали путем смены питательной среды с добавлением остеофакторов. Далее культуры клеток окрашивали ализариновым красным, интенсивность кальцификации внеклеточного матрикса измеряли с помощью спектрофотомера.
Результаты. В процессе культивирования по краям от матрицы мы наблюдали активную пролиферацию гингивальных фибробластов в присутствии экспериментальных образцов. Несмотря на то что клетки активно пролиферировали в присутствии экспериментальных образцов, их пролиферация все же была ниже, чем у контрольных клеток. Мы выявили, что интенсивность окраски ализариновым красным у образца PLA/HA оказалась выше, что свидетельствует о большей кальцификации внеклеточного матрикса.
Заключение. Таким образом, при оценке эффективности остеогенной дифференцировки клеток соединительной ткани десны на модифицированных композиционных матрицах из PLA и PLA/HA, PLGA 85:15 и PLGA 60:40 было выявлено, что клетки способны к пролиферации и дифференцировке в остеогенном направлении в присутствии полимерных пластин и могли бы применяться при проведении операций по увеличению объема костной ткани в полости рта.
Введение
Костная пластика челюстей является наиболее сложной областью в современной стоматологии и челюстно-лицевой хирургии. Костные дефекты челюстей могут возникать в результате различных причин, таких как: удаление зубов, травмы, опухолевые процессы, инфекции или врожденные аномалии. Восстановление этих дефектов является сложной задачей, требующей применения специальных техник и материалов. При восстановлении зубочелюстной системы с использованием дентальных имплантатов, качество и объем альвеолярной кости в области имплантации влияют на положение имплантата, его первичную стабильность и восстановление формы мягких тканей.
Альвеолярная кость подвергается резорбции и атрофии после потери зуба, ширина и высота альвеолярного гребня уменьшаются, и костные условия становятся недостаточными для проведения имплантации. Поэтому реконструкция альвеолярной кости в области имплантации является ключевым аспектом в стоматологии. Согласно текущим статистическим данным, ежегодно выполняется примерно 2,2 миллиона операций по аугментации костной ткани. Несмотря на большое количество техник, проблема атрофии челюсти остается актуальной, и количество таких операций увеличивается каждый год на 13%. Мы стремимся уменьшить осложнения, риски и улучшить качество работы челюстно-лицевых хирургов.
На данный момент существует множество методов аугментации костной ткани, известных во всем мире, таких как: техника направленной регенерации кости (НКР), аугментация с использованием политетрафторэтиленовых (PTFE) мембран, коллагеновых биорезорбируемых мембран, титановых сеток, аугментация аутоблоками и другие. Однако основным недостатком применения готовых титановых каркасов является интраоперационной этап адаптации мембраны в соответствии с индивидуальными размерами дефекта пациента, что значительно увеличивает время проведения операции, а также может повлиять на развитие осложнений.
Технология CAD/CAM может быть использована для планирования каждого случая и создания индивидуальных титановых каркасов для аугментации костей. Благодаря тому что они являются персонализированными, время операции сокращается, доктору не нужно адаптировать продукт в полости рта. Более того, мембрана закрепляется с учетом архитектоники кости и анатомической структуры пациента, что значительно снижает риски. Однако использование титановых мембран подразумевает дополнительный хирургический этап — извлечение мембраны после созревания костной ткани перед проведением имплантации.
Для улучшения качества челюстно-лицевой хирургии необходимо разработать материалы с хорошими механическими свойствами, нетоксичными и благоприятными биологическими и химическими характеристиками для изготовления мембран для реконструкции костей. Поэтому мы решили обратить внимание на индивидуальные, но биоразлагаемые мембраны. Использование биодеградируемых материалов может стать новым шагом в аугментации костной ткани челюстей. Бесспорное, наиболее важное преимущество данных мембран заключается в отсутствии необходимости в одном дополнительном хирургическом этапе — извлечение каркасов перед проведением имплантации.
Полилактид (PLA) является биоразлагаемым и биосовместимым полимером, который нашел широкое применение в медицине. Полилактид может быть использован для создания различных медицинских изделий и материалов, таких как шовный материал, имплантаты и даже 3D-напечатанные модели. Одним из главных преимуществ PLA в медицине является его способность к биорезорбции. Это означает, что после использования, PLA может раствориться в организме и выводиться из него естественным путем, без необходимости вторичной операции для удаления материала.
Сополимер полилактида и гликолида (Poly (lactic-co-glycolic acid), PLGA) — это одно из соединений, также часто использующихся в медицине. Химическое сшивание молочной и гликолиевой кислот значительно изменяет свойства полимера. Например, PLGA с соотношением мономеров молочной и гликолиевой кислот (75:25) будет иметь меньший модуль Юнга относительно PLA и большую скорость разложения. Время биорезорбции PLGA может варьировать от нескольких месяцев до нескольких лет в зависимости от соотношения мономеров и молекулярной массы полимера. Кроме того, влияние будут оказывать толщина и форма изделий, присутствие лекарственных веществ или других добавок, а также условия окружающей среды, такие как pH, температура и влажность.
Опираясь на проведенный анализ литературы, можно отметить, что скаффолды из полилактида и его производных являются перспективной альтернативой применения титановых каркасов в челюстно-лицевой области.
Цель исследования — изучить влияние разных полимерных составов индивидуальных каркасов для костной пластики на процессы пролиферации и остеогенной дифференцировки в условиях in vitro.
Материалы и методы исследования
Были подготовлены прототипы мембран из чистого полилактида (PLA, Ingeo 4032D, NatureWorks LLC, США), полилактида с добавлением 15% масс. наночастиц гидроксиапатита (HA, ГАП 85УД, ООО "НПК "Полистом", Россия), сополимеров полилактида с гликолидом (PLGA, Lattice Services 3D printing medical fi laments) с соотношениями мономеров 60:40 и 85:15.
Пластины размером 10 х 10 х 0,5 мм были подготовлены методом 3D-печати с использованием 3D-принтера BiZon Prusa i3 Steel PRO (3DiY, Russia). Температура экструдера составляла 180 °С, температура стола — 60 °С.
Мембраны были смоделированы в программе ZBush и далее изготовлены на 3D-принтере Prusa методом FDM печати с последующей стерилизацией. FDM (Fused Deposition Modeling) — это метод печати 3D-моделей, при котором пластичный материал (например, PLA) расплавляется и наносится слоями для создания объекта. FDM-печать широко используется в различных областях, таких как прототипирование, производство, медицинская технология и дизайн.
Стерилизация образцов проводилась гамма излучением (метод радиационной стерилизации с помощью потоков частиц, способных ионизировать вещество). При этом средняя доза при стерилизации радиацией равна 25 кГр (2,5 Мрад); выбор этого значения обосновывается с помощью микробиологических испытаний в соответствии с ГОСТ Р ИСО 11737-1 (рис. 1).
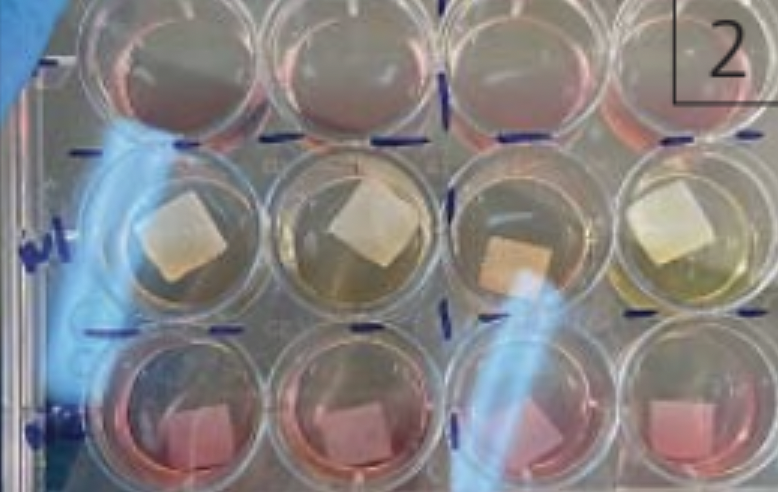
Для оценки влияния экспериментальных образцов из разного полимерного материала на процессы пролиферации и остеогенной дифференцировки клеток были использованы гингивальные фибробласты в условиях in vitro.
Задачей исследования было оценить остеогенную дифференцировку и пролиферацию клеток в присутствии образцов из разных полимерных материалов. Для этого использовался протокол in vitro, содержащий гингивальные фибробласты. Гингивальные фибробласты — мультипотентные клетки соединительной ткани десен, которые играют важную роль в поддержании целостности и функциональности десны, особенно с точки зрения восстановления и репарации тканей пародонта.
Гингивальные фибробласты в концентрации 100 тысяч клеток на лунку были посеяны на культуральный пластик и культивировались в низкоглюкозной питательной среде DMEM 1.0 (Gibco, США) с добавлением 10% фетальной бычьей сыворотки (FBS, HyClone, США), 2 мМ L-глутамина (Gibco, США), 100 ед/мл пенициллина/стрептомицина (Gibco, США), при 37 °C, 5% CO2. После адгезии клеток к культуральному пластику в лунки помещали экспериментальные образцы композиционных пластин PLA No1-4.
Остеогенную дифференцировку индуцировали путем смены питательной среды на соответствующую с добавлением остеофакторов 50 мкг/мл аскорбиновой кислоты, 0,1 мкМ дексаметазона и 10 мМ
β-глицерофосфата. В качестве контроля использовали клеточные культуры гингивальных фибробластов, культивировавшиеся в присутствии матриц в контрольной питательной среде, без добавления остеофакторов, а также клетки, культивировавшиеся на пластике в контрольной и остеогенной среде в отсутствии композиционных материалов. Клетки культивировали в течение 20 дней. Питательную среду меняли 2 раза в неделю. Предоставленные экспериментальные образцы No 1, 2, 3 и 4 представляли собой объемные непрозрачные пористые матрицы, которые занимали большую часть объема лунки, в связи с чем прижизненно оценить пролиферацию и жизнеспособность клеток под самими матрицами в процессе культивирования нам не удалось.
По истечении времени культивирования, культуры клеток окрашивали ализариновым красным с целью оценки влияния экспериментальных образцов на остеогенную дифференцировку гингивальных фибробластов, которые культивировались в присутствии матриц. Клетки промывали фосфатносолевым буфером (Биолот, Россия) и фиксировали 70% этанолом в течение 1 часа, дважды отмывали дистиллированной водой и после инкубировали в растворе ализаринового красного (Sigma, США) в соответствии с протоколом производителя, в течение 20-30 минут при комнатной температуре. Для визуализации отложений фосфатов кальция, окрашенные ализариновым красным клетки фотографировали с помощью инвертированного микроскопа (Leica, Германия).
Для количественного анализа интенсивности кальцификации внеклеточного матрикса измеряли спектрофотометрические показатели с помощью модифицированной методики экстракции ализаринового красного. К культурам клеток, окрашенных ализариновым красным, добавляли 10% раствор уксусной кислоты и инкубировали в течение 10 минут при комнатной температуре, интенсивность окраски измеряли на спектрофотометре (Fluorofot Charity, Россия) при необходимой длине волны — 450 нм.
Результаты исследования
В процессе культивирования по краям от матрицы мы наблюдали активную пролиферацию гингивальных фибробластов в присутствии экспериментальных образцов, что свидетельствует о том, что пластины нетоксичны и не способствуют гибели клеток (рис. 3, 4).
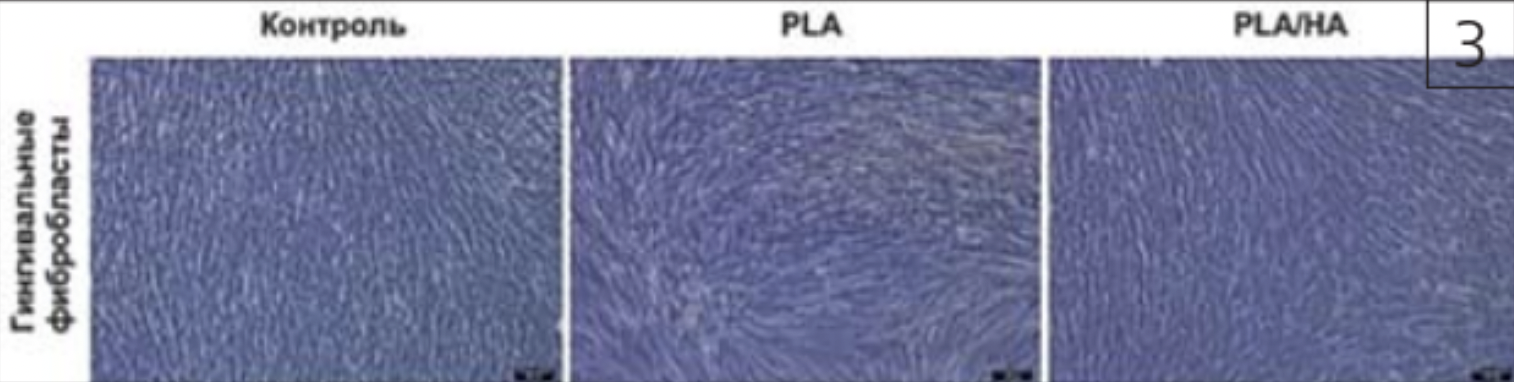
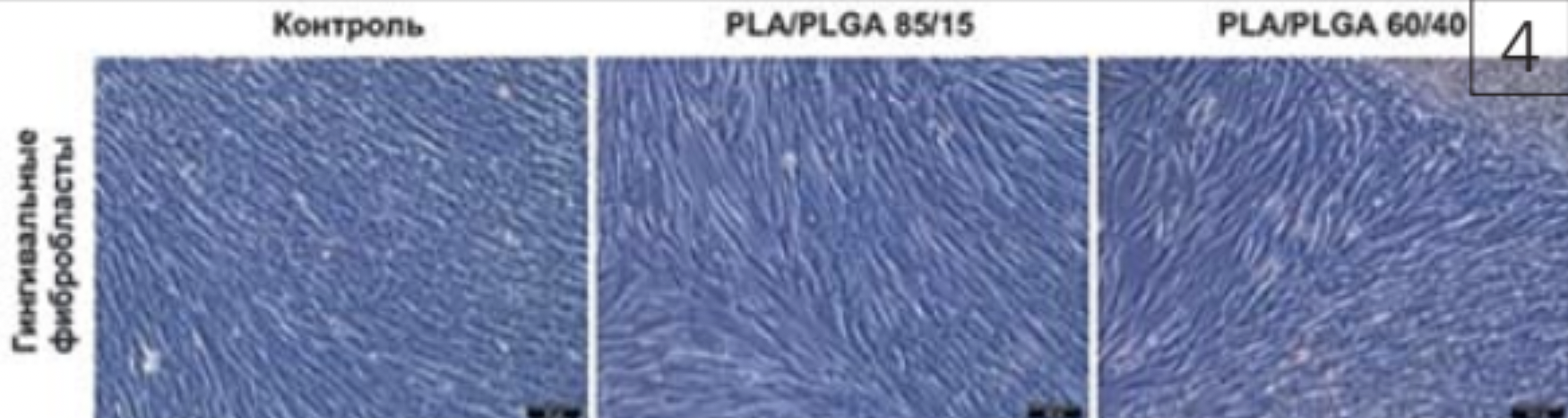
Несмотря на то что клетки активно пролиферировали в присутствии экспериментальных образцов, их пролиферация все же была ниже, чем у контрольных клеток, особенно у образца No3. В процессе культивирования нами было сделано следующее наблюдение: питательная среда в присутствии образца No3 изменяла свой цвет, что свидетельствует об изменении pH питательной среды. Предполагаем, что именно это могло негативно повлиять на пролиферацию клеток.
Для выполнения поставленной задачи и анализа эффективности остеогенной дифференцировки гингивальных фибробластов с помощью окраски ализариновым красным, из лунок с клетками необходимо было достать экспериментальные образцы.
Образцы No1 и 2 не подверглись изменениям, однако образцы No3 и 4, в связи с тем что находились в питательной среде длительный срок, набухли и изменили свою первоначальную форму — стали мягкими и пластичными. Вследствие этого при извлечении матриц из лунок они повредили значительную часть монослоя клеток, что сильно усложнило дальнейший анализ. Однако на неповрежденных участках нам все же удалось оценить влияние экспериментальных образцов на остеогенную дифференцировку гингивальных фибробластов, которые культивировались в присутствии пластин.
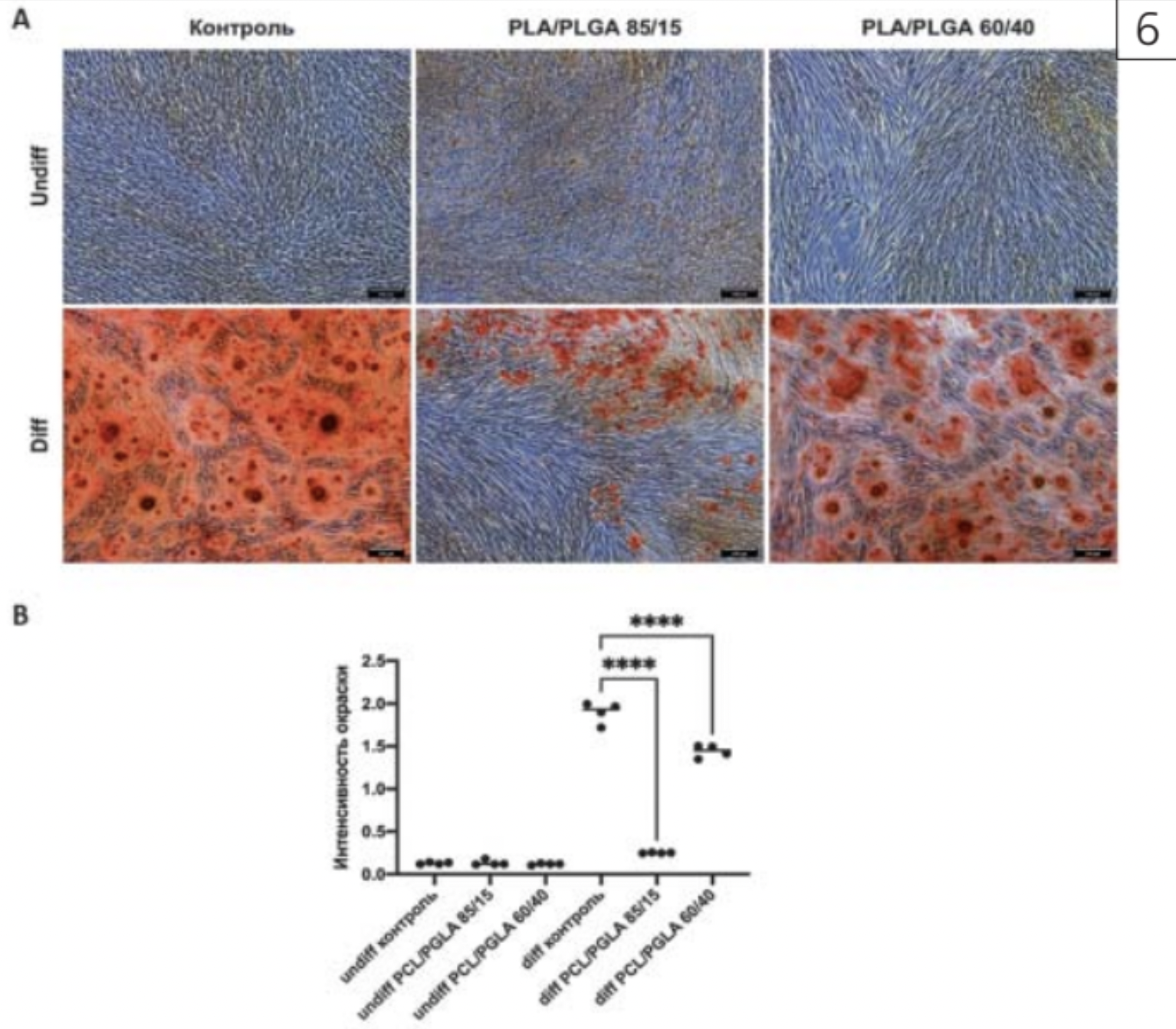
Таким образом, гингивальные фибробласты, которые культивировались в остеогенных условиях в присутствии образов No1, No2, No3 и No4, способны к остеогенной дифференцировке (рис. 5, 6).
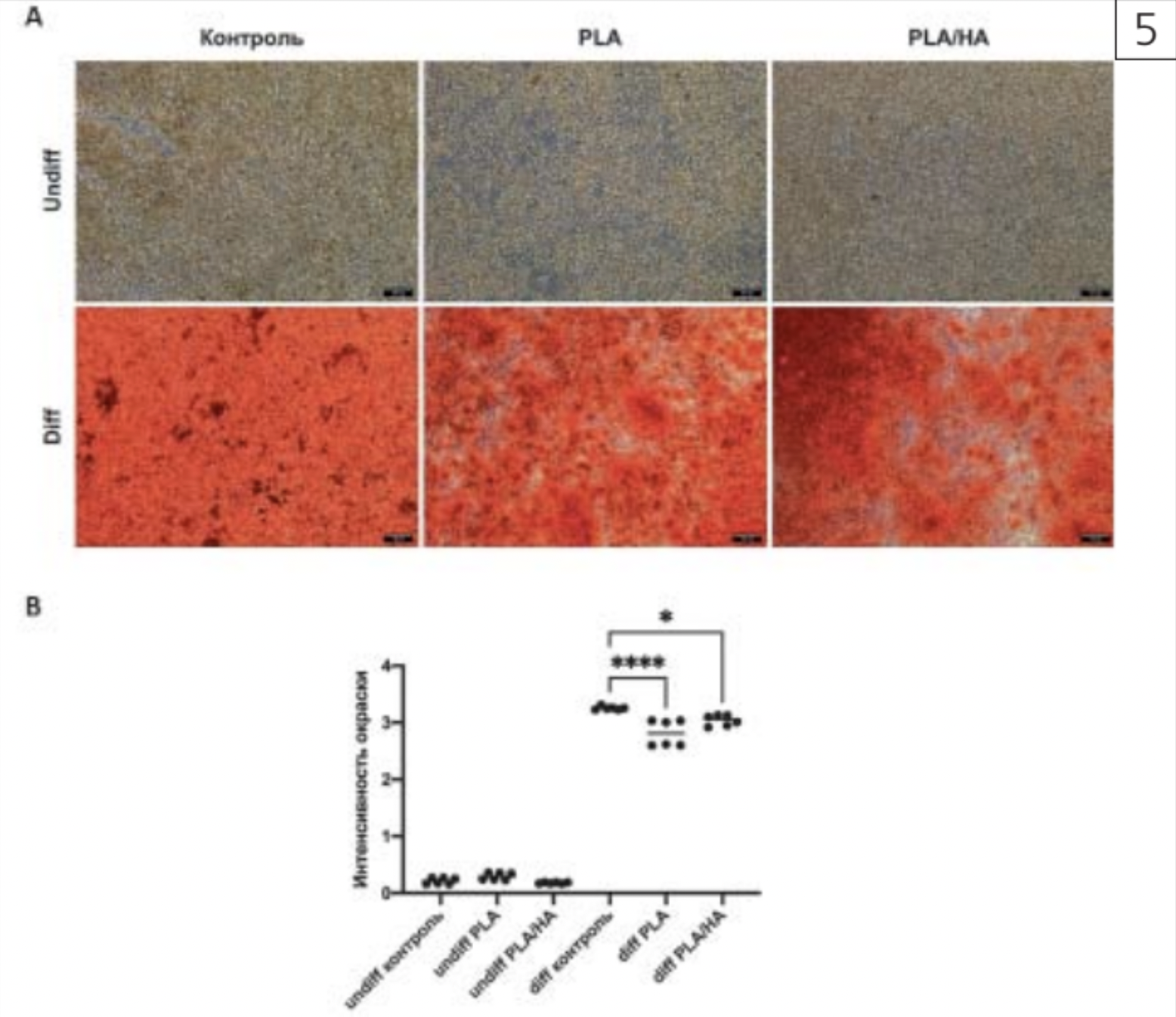
Но усиления индукции остеогенной дифференцировки в присутствии пластин, относительно контрольных клеток, которые культивировались в среде с добавлением остеофакторов в отсутствии композиционных материалов, мы не обнаружили. Однако при сравнении образцов No1 и No2 относительно друг друга, мы выявили, что интенсивность окраски ализариновым красным у образца No2 оказалась выше, чем у образца No1, что свидетельствует о большей кальцификации внеклеточного матрикса (рис. 5 В). Было выявлено, что матрицы с добавлением частиц гидроксиапатита увеличивают степень образования кальцифицированного внеклеточного матрикса у гингивальных фибробластов.
Однако при сравнении образцов No3 и No4 относительно друг друга, мы выявили, что интенсивность окраски ализариновым красным у образца No4 оказалась значительно выше, чем у образца No3, что свидетельствует о большей кальцификации внеклеточного матрикса (рис. 6 В). Мы предполагаем, что изменение процентного соотношения PLGA относительно PLA в составе пластины может способствовать увеличению степени образования кальцифицированного внеклеточного матрикса у гингивальных фибробластов.
Таким образом, при оценке эффективности остеогенной дифференцировки клеток соединительной ткани десны на модифицированных композиционных матрицах из PLA и PLA/HA, PLGA 85/15 и PLGA 60/40 было выявлено, что клетки способны к пролиферации и дифференцировке в остеогенном направлении в присутствии полимерных пластин. При этом, по-видимому, частицы гидроксиапатита в составе матриц могут влиять на степень остеогенной дифференцировки клеток. Также изменение процентного соотношения полимеров относительно друг друга, по-видимому, может влиять как на пролиферацию, так и на степень остеогенной дифференцировки клеток. Однако, несмотря на это, степень их пролиферации и синтеза кальцифицированного внеклеточного матрикса ниже, чем в контрольных клетках.
Выводы
- Таким образом, можно сделать вывод, что модифицированные композиционные матрицы из PLA, PLA/HA, PLGA 85/15 и PLGA 60/40 являются перспективными медицинскими изделиями, которые могли бы применяться при проведении операций по увеличению объема костной ткани в полости рта.
- Прототипы мембран из представленных составов нетоксичны и не способствуют гибели клеток.
- Пластины с добавлением гидроксиапатита способствуют остеогенной дифференцировке клеток, по сравнению с другими образцами, но при этом они не достигают такого уровня пролиферации и синтеза внеклеточного матрикса, как контрольные клетки.
- Результаты сравнения образцов сополимеров PLGA с различной концентрацией кислот (60/40, 85/15) позволяют сделать вывод, что изменение соотношения гликолевой кислоты относительно молочной в составе матрицы может оказывать влияние на степень образования кальцифицированного внеклеточного матрикса.
- Дальнейшие исследования в этом направлении могут быть направлены на оптимизацию состава мембран для достижения максимального эффекта в стимуляции остеогенеза, изучения времени биорезорбции материалов в условиях in vivo.
Авторы
А.И.Яременко, Е.А.Зерницкая, А.П.Реутова, А.Б.Малашичева, Д.А.Переплетчикова, А.И.Зимина, П.А.Ковалева, Д.И.Степанова
Список литературы
- Гордиенко М.Г., Каракатенко Е.Ю., Меньшутина Н.В., Актянова А.В., авторы; ФГБОУ ВО «РХТУ им. Д.И. Менделеева», патентообладатель. Биосовместимый биоразлагаемый скаффолд на основе полимерного композита, содержащего наночастицы гидроксиапатита. Пат. 2756551 Рос. Федерация. Опубл. 01.10.2021.
- Ferràs-Tarragó J., Sabalza-Baztán O., Sahuquillo-Arce J.M., Angulo-Sánchez M.Á., Amaya-Valero J., De-La-Calva Ceinos C., Baixauli-García F. Security of 3D-printed polylactide acid piece sterilization in the operating room: a sterility test // European Journal of Trauma and Emergency Surgery. — 2022. — Vol. 48, No 5. — P. 3895–3900. https://doi.org/10.1007/s00068-020-01564-1
- Hua N., Ti V.L., Xu Y. Biodegradable effect of PLGA membrane in alveolar bone regeneration on beagle dog // Cell Biochem Biophys. — 2014. — Vol. 70, No 2. — P. 1051–1055. https://doi.org/10.1007/s12013-014-0022-5
- Ikawa H., Moroi A., Yoshizawa K., Saida Y., Hotta A., Tsutsui T., Fukaya K. et al. Bone regeneration enhancement by ultra-violet (UV) treatment for uHA/PLLA absorbable mesh // Journal of Cranio-Maxillo-Facial Surgery. — 2017. — Vol. 45, No 5. — P. 634–641. https://doi.org/10.1016/j.jcms.2017.02.001
- Kanno T., Sukegawa S., Furuki Y., Nariai Y., Sekine J. Overview of innovative advances in bioresorbable plate systems for oral and maxillofacial surgery // Japanese Dental Science Review. — 2018. — Vol. 54, No 3. — P. 127–138. https://doi.org/10.1016/j.jdsr.2018.03.003
- Lobov A., Kuchur P., Khizhina A., Kotova A., Ivashkin A., Kostina D. et al. Mesenchymal Cells Retain the Specificity of Embryonal Origin During Osteogenic Differentiation // Stem Cells. — 2024. — Vol. 42, No 1. — P. 76–89. https://doi.org/10.1093/stmcls/sxad081
- Matsuo A., Chiba H., Takahashi H., Toyoda J., Abukawa H. Clinical application of a custom-made bioresorbable raw particulate hydroxyapatite/poly-L-lactide mesh tray for mandibular reconstruction // Odontology. — 2010. — Vol. 98, No 1. — P. 85–88. https://doi.org/10.1007/s10266-009-0111-x
- Ngo H.X., Bai Y., Sha J., Ishizuka S., Toda E., Osako R. et al. A Narrative Review of u-HA/PLLA, a Bioactive Resorbable Reconstruction Material: Applications in Oral and Maxillofacial Surgery // Materials (Basel). — 2021. — Vol. 15, No 1. — P. 150. https://doi.org/10.3390/ma15010150
- Pérez Davila S., González Rodríguez L., Chiussi S., Serra J., González P. How to Sterilize Polylactic Acid Based Medical Devices? // Polymers (Basel). — 2021. — Vol. 13, No 13. — P. 2115. https://doi.org/10.3390/polym13132115
- Shea G.K., Wu K.L., Li I.W., Leung M.F., Ko A.L., Tse L. et al. A review of the manufacturing process and infection rate of 3D-printed models and guides sterilized by hydrogen peroxide plasma and utilized intra-operatively // 3D Printing in Medicine. — 2020. — Vol. 6, No 1. — P. 7. https://doi.org/10.1186/s41205-020-00061-w
- Sun F., Sun X., Wang H., Li C., Zhao Y., Tian J., Lin Y. Application of 3D-Printed, PLGA-Based Scaffolds in Bone Tissue Engineering // International Journal of Molecular Sciences. — 2022. — Vol. 23, No 10. — P. 5831. https://doi.org/10.3390/ijms23105831
- Tolstunov L., Hamrick J.F.E., Broumand V., Shilo D., Rachmiel A. Bone Augmentation Techniques for Horizontal and Vertical Alveolar Ridge Deficiency in Oral Implantology // Oral and Maxillofacial Surgery Clinics of North America. — 2019. — Vol. 31, No 2. — P. 163–191. https://doi.org/10.1016/j.coms.2019.01.005
- Zhao D., Zhu T., Li J., Cui L., Zhang Z., Zhuang X., Ding J. Poly(lactic-co-glycolic acid)-based composite bone-substitute materials // Bioactive Materials. — 2020. — Vol. 6, No 2. — P. 346–360. https://doi.org/10.1016/j.bioactmat.2020.08.016
- Zhao R., Yang R., Cooper P.R., Khurshid Z., Shavandi A., Ratnayake J. Bone Grafts and Substitutes in Dentistry: A Review of Current Trends and Developments // Molecules. — 2021.
