Histomorfometría del hueso tras la exposición intencionada de membranas d-PTFE no reabsorbibles o regeneración ósea guiada para el tratamiento de defectos óseos alveolares post-extracción con restauraciones soportadas por implantes: un ensayo control...
Traducción automática
El artículo original está escrito en idioma EN (enlace para leerlo) .
Resumen
Objetivo: El objetivo del presente estudio fue investigar el examen histológico cuantitativo del hueso reconstruido con membrana de politetrafluoroetileno de alta densidad no reabsorbible (d-PTFE), dejado intencionadamente expuesto en los alvéolos post-extracción injertados con material óseo anorgánico, y retirado después de cuatro semanas, en comparación con la extracción y regeneración ósea guiada (GBR), realizada dos meses después.
Materiales y Métodos: Este estudio fue diseñado como un ensayo controlado aleatorio multicéntrico de diseño de grupos paralelos. Los pacientes fueron seleccionados y tratados de manera consecutiva en tres centros en Italia. Los pacientes recibieron aleatoriamente la membrana d-PTFE no reabsorbible intencionadamente expuesta (grupo A), o regeneración ósea guiada (grupo B), para tratar defectos óseos alveolares post-extractivos con restauraciones soportadas por implantes. Los resultados fueron: el fallo del implante, cualquier complicación mecánica y biológica, la satisfacción del paciente, y la evaluación cualitativa e histomorfométrica de las muestras óseas recolectadas.
Resultados: Dieciocho pacientes fueron inscritos consecutivamente en el ensayo. De estos, seis de 18 pacientes eran hombres. Todos los pacientes incluidos fueron tratados de acuerdo con las intervenciones asignadas, y no hubo deserciones. No se experimentó falla del implante ni complicaciones, y todos los pacientes estaban completamente satisfechos con la función y estética de su restauración soportada por implantes, sin diferencias entre grupos. El análisis morfológico no reveló signos de reacción tisular, como fibrosis o necrosis. El hueso regenerado estaba bien mineralizado en ambos grupos, pero parecía más maduro en el grupo B que en el grupo A. Tres muestras mostraron un número mínimo de linfocitos. Varios vasos sanguíneos de pequeño tamaño ocupaban los espacios medulares, donde el tejido resultó ser más maduro, indicando la actividad del tejido en progreso. La evaluación histomorfométrica no mostró diferencias estadísticamente significativas en las fracciones de volumen de tejido entre los dos grupos de pacientes.
Conclusiones: Con la limitación del presente estudio, la reconstrucción de la placa bucal con una membrana no reabsorbible intencionadamente expuesta es un procedimiento efectivo y fácil para regenerar una placa ósea bucal reabsorbida, reduciendo la necesidad de regeneración ósea guiada.
Introducción
La pérdida de hueso alveolar puede atribuirse a una variedad de factores, como patología endodóntica, periodontitis, trauma facial y maniobras agresivas durante las extracciones. Además, después de la extracción dental, ocurre una cascada de eventos biológicos, que generalmente resulta en cambios anatómicos locales significativos, incluyendo la reducción de la altura y el ancho del reborde residual. La pérdida ósea horizontal es generalmente la mayor y ocurre con más frecuencia en el lado bucal. Se pueden lograr tasas de éxito de implantes favorables y respuestas de tejidos peri-implantarios al colocar implantes inmediatamente después de la extracción dental; sin embargo, se observó la continua recesión del tejido gingival facial. Para mejorar la previsibilidad estética de los implantes post-extracción, se han realizado varios estudios y revisiones sistemáticas para evaluar la eficacia de diferentes enfoques de llenado de alvéolos que involucran diferentes materiales de injerto, con o sin membranas de barrera. En estos estudios, se ha utilizado una plétora de biomateriales, incluyendo hueso autólogo, sustitutos óseos (aloinjertos, xenoinjertos y aloplásticos), y productos derivados de sangre autóloga, así como agentes bioactivos. Sin embargo, ensayos clínicos recientes y revisiones sistemáticas no encontraron evidencia de que un biomaterial y una membrana de barrera fueran superiores a los otros. Con las limitaciones de este estudio, el uso de membranas de politetrafluoroetileno no reabsorbible de alta densidad (d-PTFE) fue seguro y predecible, particularmente en términos de ancho de tejido queratinizado.
Los mismos estudios fomentan ensayos controlados aleatorios bien realizados.
Elian et al. propusieron una clasificación simplificada de los alvéolos y un enfoque no invasivo para el injerto y manejo de alvéolos cuando hay tejido blando presente, pero la placa bucal está comprometida (Tipo II). Los autores utilizaron membranas de colágeno y materiales de injerto para el tratamiento de alvéolos tipo II. Una revisión sistemática reciente concluyó que las membranas de PTFE protegen el material de injerto y/o el coágulo de curación inicial de la contaminación bacteriana, lo que lleva a una regeneración exitosa sin un riesgo significativo de infección.
El objetivo del presente ensayo controlado aleatorio fue investigar el examen histológico cuantitativo del hueso reconstruido con membrana de d-PTFE, dejado intencionalmente expuesto en alvéolos post extracción injertados con material óseo anorgánico, y retirado después de cuatro semanas, frente a la extracción y regeneración ósea guiada (GBR), realizada dos meses después. La hipótesis nula era que no había diferencias estadísticas respecto a la evaluación cualitativa e histomorfométrica de las muestras entre grupos. La hipótesis nula fue probada contra la hipótesis alternativa de diferencia. La presente investigación fue redactada de acuerdo con las directrices de CONSORT.
Materiales y Métodos
Este estudio fue diseñado como un ensayo piloto, multicéntrico y controlado aleatoriamente de diseño de grupos paralelos, con el objetivo de evaluar la histomorfometría del hueso y los parámetros clínicos de pacientes con dientes irrecuperables mandibulares y maxilares ubicados entre los premolares, que requieren una restauración de corona única soportada por implante con retraso. Los pacientes fueron seleccionados y tratados de manera consecutiva en tres centros en Italia desde noviembre de 2018 hasta septiembre de 2020.
Tres clínicos realizaron tanto procedimientos quirúrgicos como prostéticos. La calibración de los cirujanos aseguró que cada uno realizara dos casos clínicos adicionales, con el fin de estimar y reducir los riesgos quirúrgicos potenciales. Este estudio se llevó a cabo de acuerdo con los principios establecidos en la Declaración de Helsinki de 1964 para la investigación biomédica que involucra sujetos humanos, según enmendada en la 64ª Asamblea General de la WMA, Fortaleza, Brasil, octubre de 2013, y recibió aprobación ética del “Comité Ético Lazio 1”. Número de protocolo 23/CE Lazio 1, del 7 de enero de 2020. Los pacientes fueron debidamente informados sobre la naturaleza del estudio. Se obtuvo un formulario de consentimiento informado por escrito para los procedimientos quirúrgicos y prostéticos, así como para el uso de los datos clínicos y radiológicos, para cada paciente antes de que comenzaran los tratamientos.
Criterios de Inclusión y Exclusión
Cualquier sujeto que requiera al menos una restauración única soportada por implante entre premolares, para reemplazar un diente fallido con una placa ósea bucal dañada pero con la arquitectura de tejido blando mantenida (Tipo II según Elian et al.), que tenga al menos 18 años y que pueda firmar un formulario de consentimiento informado, fue considerado elegible para este estudio y se inscribió de manera consecutiva. Los dientes sin esperanza se juzgaron de la siguiente manera: involucramiento de la furcación > II; movilidad > II; PPD > 6 mm con el porcentaje de pérdida ósea alveolar/longitud de la raíz ≥70%; patología radiográfica persistente y/o síntomas (por ejemplo, dolor, fístula, absceso) de origen endodóntico y un pronóstico incierto; restaurabilidad.
Cada paciente contribuyó solo con un procedimiento. El sitio seleccionado debía tener dientes/implantes adyacentes. Los criterios de exclusión fueron:
- Contraindicaciones generales a la cirugía oral (como ASA III y IV);
- Fumadores empedernidos (≥ 10 cigarrillos/día);
- Adicción al alcohol o drogas;
- Infecciones agudas y crónicas en el sitio destinado para la colocación del implante;
- Pobre higiene oral (sangrado en toda la boca e índice de placa en toda la boca superior al 25%);
- Embarazo o lactancia;
- Terapia psiquiátrica;
- Pacientes tratados o en tratamiento con bisfosfonatos amino intravenosos;
- Radioterapia previa de la región oral y maxilofacial en los últimos 5 años;
- Pacientes incapaces de comprometerse con el seguimiento programado.
Procedimientos Clínicos
Los pacientes potencialmente elegibles fueron evaluados clínicamente y se registraron sus historiales médicos. Durante la visita, se obtuvieron radiografías periapicales preoperatorias, modelos de estudio y fotografías, y se registró el examen periodontal.
Los pacientes se sometieron a una higiene oral profesional antes de la cirugía y recibieron terapia profiláctica antiséptica (enjuague bucal de clorhexidina al 0.2% un minuto antes de la cirugía) y terapia antibiótica (dos gr de amoxicilina y ácido clavulánico, o clindamicina 600 mg si eran alérgicos a la penicilina, una hora antes de la cirugía). Todos los pacientes fueron tratados bajo anestesia local utilizando clorhidrato de articaína con adrenalina 1:100,000 (Orabloc, Pierrel, Milán, Italia). Las extracciones dentales se realizaron sin colgajo, de la manera más atraumática posible. Los dientes multirradiculares se seccionaron en la furcación y las raíces se extrajeron individualmente. Posteriormente, el alvéolo de extracción residual se lavó con solución salina y se desbridó a fondo de tejido de granulación y fibras residuales del ligamento periodontal. Finalmente, se evaluó la pared ósea con la ayuda de una sonda periodontal (PCPUNC156, Hu-Friedy). Después, los pacientes que cumplieron con todos los criterios de inclusión fueron inscritos de manera definitiva, y un asistente independiente cegado abrió un sobre sellado numerado secuencialmente correspondiente al número de reclutamiento del paciente para conocer el grupo de asignación.
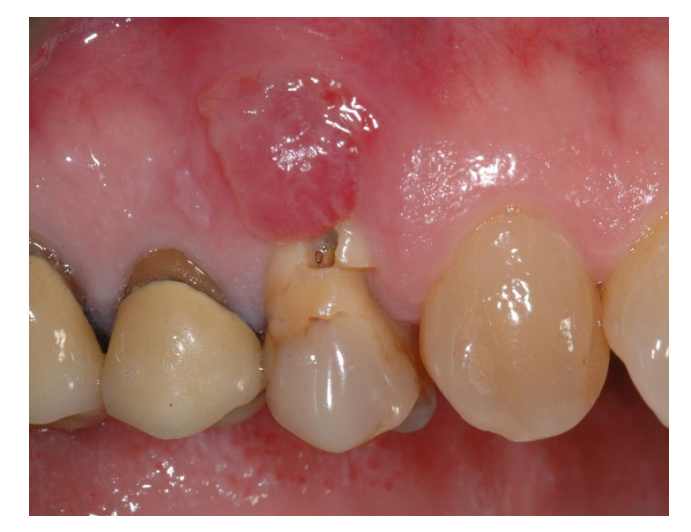
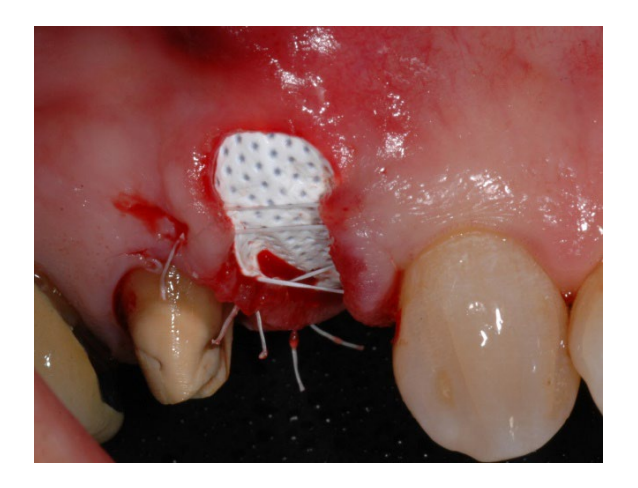
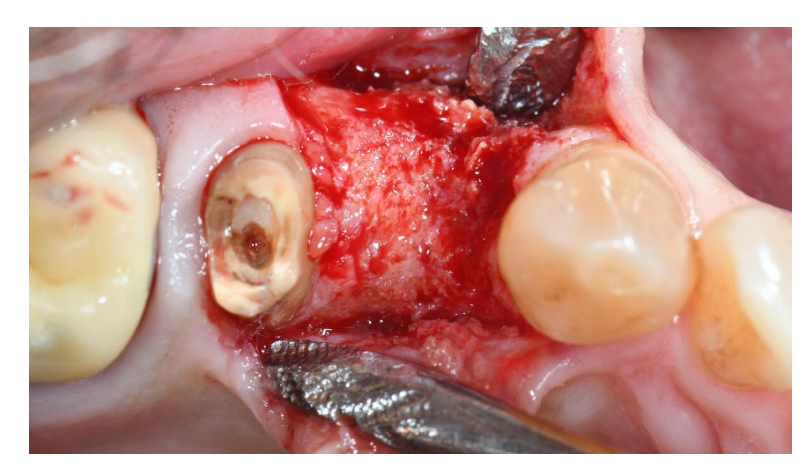
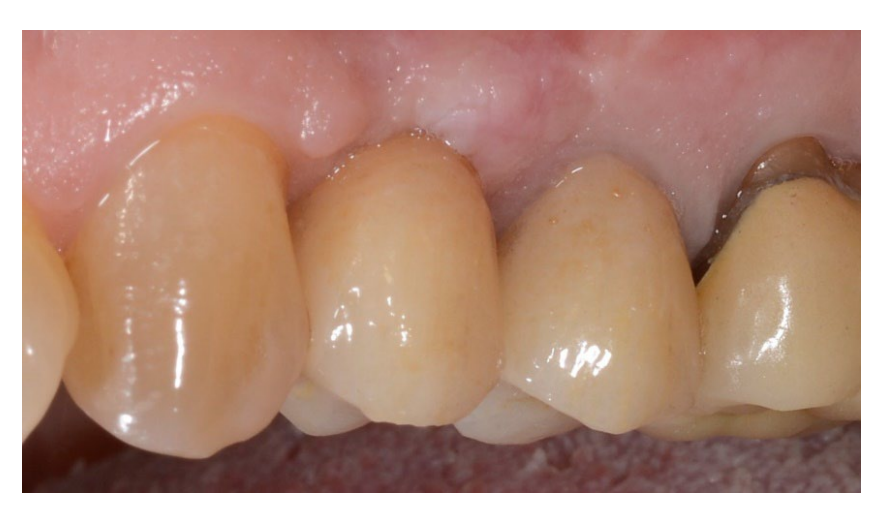
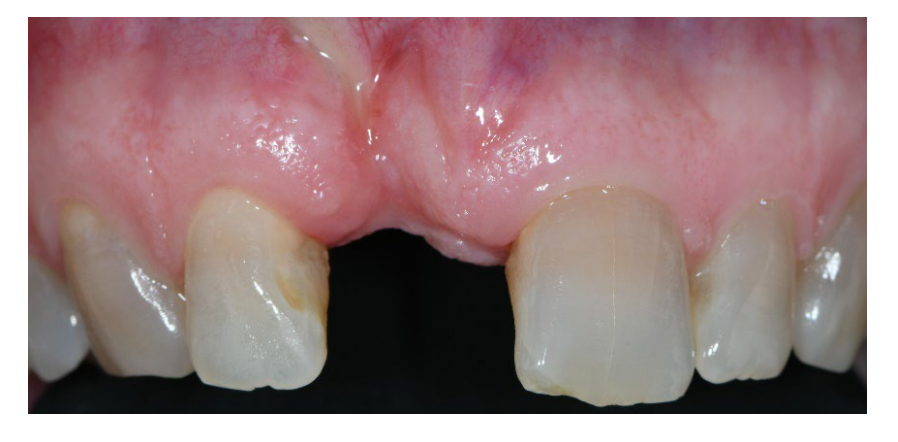
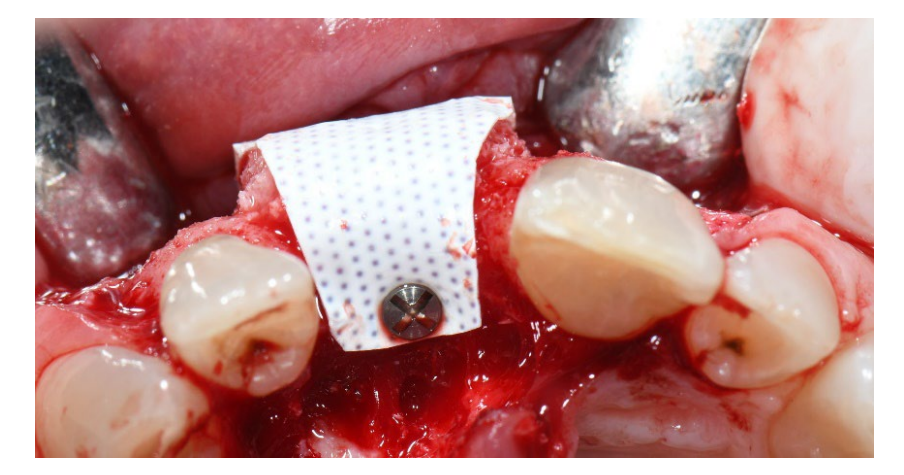
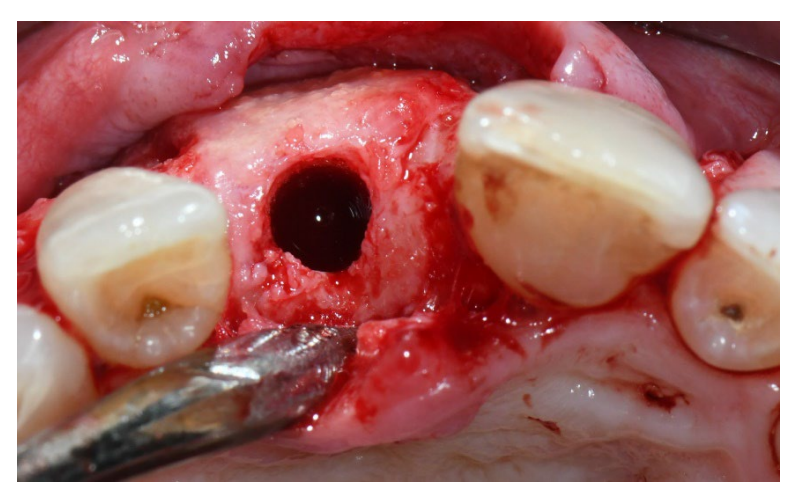
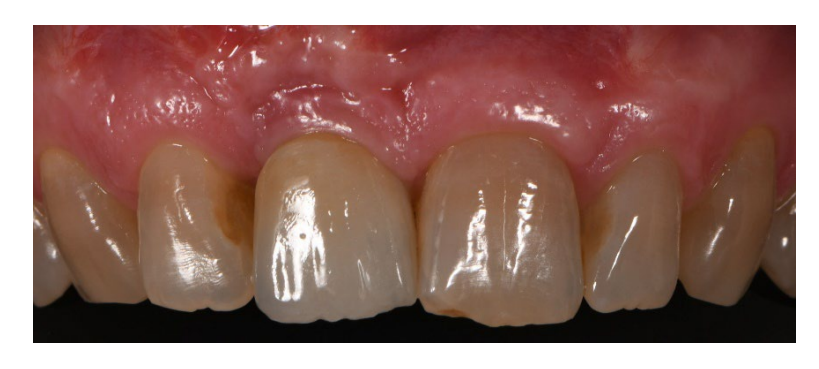
En el grupo A, la preservación del alvéolo con una membrana de d-PTFE no reabsorbible intencionalmente expuesta (grupo de prueba, Figuras 1–4), el alvéolo residual fue injertado con material óseo anorgánico de origen porcino (partículas de 0.25–1 mm, Zcore, DeOre s.r.l., Negrar [Vr], Italia). Luego, se moldeó una membrana de politetrafluoroetileno denso y no reabsorbible (d-PTFE) (Cytoplast TXT1224, DeOre) de acuerdo con las dimensiones del alvéolo residual, y se insertó en un bolsillo bucal y lingual. Finalmente, se colocó una sutura horizontal en colchón (Cytoplast PTFE Suture 4-0, DeOre) para asegurar la membrana y estabilizarla a los márgenes de los tejidos blandos. La aplicación de la membrana de d-PTFE no reabsorbible no requirió cierre primario mediante avance de colgajo bucal. Las suturas se retiraron entre 10 y 14 días después de la cirugía, y la membrana de d-PTFE no reabsorbible se retiró entre la cuarta y la quinta semana después de la cirugía. Después de eso, la herida se dejó sanar durante aproximadamente cinco meses, permitiendo el proceso de reepitelización.
En el grupo B, GBR (grupo de control, Figuras 5–8), solo se insertó una esponja de fibrina en el alvéolo para estabilizar el coágulo de sangre.
En ambos grupos, se administró 1 g de amoxicilina (o 300 mg de clindamicina) cada 12 h durante seis días después de la extracción dental y la reconstrucción ósea. Se prescribieron paracetamol 500 mg más codeína 30 mg según fuera necesario. Se instruyó a los pacientes que no los tomaran en ausencia de dolor. Se prescribió un spray de clorhexidina al 0.2% dos veces al día durante dos y cinco semanas en los grupos A y B, respectivamente. Se recomendó una dieta blanda durante dos semanas después de los procedimientos quirúrgicos en ambos grupos.
En el grupo B, ocho semanas después de la extracción dental, se realizó una incisión intrasulcular utilizando una hoja Bard-Parker no. 15C, y se elevó un colgajo de grosor completo más allá de la unión mucogingival y al menos 5 mm más allá del defecto óseo. Se realizaron dos incisiones verticales al menos a un diente de distancia del área a ser aumentada. Se realizaron múltiples agujeros de decorticación en el sitio receptor con una fresa redonda. El alvéolo residual se injertó con partículas de material óseo anorgánico esponjoso de origen porcino (Zcore, DeOre). Luego, se moldeó una membrana de colágeno (Cytoplast RTM Collagen, DeOre) de acuerdo con el defecto óseo regenerado y se fijó con tres a cinco pines de titanio (Supertack, MCbio s.r.l., Lomazzo, Italia), en los lados bucal y lingual/palatino. La membrana se recortó al volumen total del injerto, uno a dos milímetros antes de la superficie de los dientes adyacentes. Se realizó una incisión periosteal entre las dos incisiones verticales para permitir un cierre completamente libre de tensión del colgajo. Los colgajos se suturaron en dos capas para evitar la exposición de la membrana (Cytoplast PTFE Suture 4-0). Primero se colocaron suturas de colchón horizontales a 4 mm de la línea de incisión; luego, se colocaron suturas interrumpidas simples para cerrar los bordes del colgajo. Las incisiones verticales se suturaron con suturas interrumpidas simples. Las suturas interrumpidas simples se retiraron entre 10 y 14 días después de la cirugía, y las suturas de colchón se retiraron de dos a tres semanas después de la cirugía. Se administró 1 g de amoxicilina (o 300 mg de clindamicina) cada 12 h durante ocho días después de la extracción dental y la reconstrucción ósea. Se prescribieron paracetamol 500 mg más codeína 30 mg según fuera necesario. Se instruyó a los pacientes que no los tomaran en ausencia de dolor.
Se prescribió un spray de clorhexidina al 0.2% dos veces al día durante dos y cinco semanas en los grupos A y B, respectivamente. Se recomendó una dieta blanda durante 2 semanas después de los procedimientos quirúrgicos en ambos grupos.
En ambos grupos, seis a ocho meses después de la extracción dental (grupo A y B, respectivamente), se colocaron implantes dentales (Premium, Suecia y Martina, Due Carrare, PD, Italia). En ninguno de los casos fue necesario realizar una GBR adicional. La cantidad de hueso se consideró suficiente para colocar un implante de 3.8 mm de diámetro y 10 a 11.5 mm de longitud. El diseño del colgajo se realizó de acuerdo con el escenario clínico y los requisitos del paciente. Antes de la preparación del sitio del implante, se utilizó una fresa trepanadora calibrada con un diámetro externo de 3.0 mm para recoger una muestra de núcleo para análisis histológico. Los implantes se sumergieron durante tres meses. Tres meses después de la colocación del implante, se entregó una restauración temporal retenida por tornillo. Finalmente, dos a tres meses después de la carga inicial, se entregó una restauración definitiva, retenida por tornillo, CAD/CAM, libre de metal. Se ajustó la oclusión y se programaron visitas de seguimiento cada cuatro meses.
Medidas de Resultado
- El fallo del implante se definió como movilidad del implante y/o cualquier infección que dictara la extracción del implante, fractura del implante, o cualquier otra complicación mecánica que haga que el implante sea inútil. Además, la estabilidad de cada implante se midió manualmente apretando el tornillo del pilar en la entrega de coronas definitivas, o evaluando la estabilidad de la corona soportada por el implante utilizando el mango de dos instrumentos metálicos en cada seguimiento.
- Cualquier complicación mecánica y biológica se registró durante todo el período de seguimiento. Los mismos operadores calibrados, que realizaron todos los procedimientos quirúrgicos y prostéticos, evaluaron los fallos del implante y las complicaciones.
- La satisfacción del paciente fue evaluada por operadores cegados en cada centro, que no habían estado involucrados previamente en el estudio. En la entrega de coronas definitivas, el evaluador independiente de resultados preguntó al paciente las siguientes preguntas (respuestas posibles: “sí” o “no”):
- ¿Está satisfecho con la función de su diente soportado por implante?
- ¿Está satisfecho con el resultado estético de su diente soportado por implante?
- ¿Se sometería a la misma terapia nuevamente?
- Se realizaron análisis cuantitativos y cualitativos en muestras anonimizadas por un patólogo cegado. Evaluación cualitativa e histomorfométrica. Después de la recolección, las muestras óseas se fijaron en formalina al 10%. Las muestras se deshidrataron con una escala de etanol creciente. Después de la deshidratación, las muestras se infiltraron con una resina de metacrilato y posteriormente se incrustaron en resina (Technovit 7200, Bio Optica, Milán). Todos los especímenes se polimerizaron utilizando una máquina de polimerización (Exakt 520, Exakt Norderstedt, Alemania). Los bloques obtenidos se cortaron mediante una máquina de sierra con una hoja de diamante (Micromet, Remet, Bolonia, Italia). Las secciones se montaron en portaobjetos de plástico utilizando una máquina de pegado (Exakt 402, Exakt Norderstedt, Alemania) y una resina de pegado (Technovit 7210, Bio Optica, Milán, Italia) y luego se lijaron a un grosor de 100 µm utilizando una máquina de molienda (LS2 Remet, Bolonia, Italia). Se obtuvieron dos secciones longitudinales representativas para cada muestra, teñidas con Azul de Toluidina y Amarillo de Pironina para resaltar las diferentes fases de mineralización ósea, y se adquirieron digitalmente a una magnificación total de 400× utilizando un escáner de alta resolución (Nanozoomer S60, Hamamatsu).
- La evaluación cualitativa tuvo como objetivo detectar la cantidad de infiltrado de tejido inflamatorio, fibroso y adiposo y eventuales áreas de necrosis siguiendo la indicación reportada por la norma ISO 10993. La evaluación histomorfométrica de las fracciones de volumen de tejido se realizó utilizando el método estereológico. Se utilizó una cuadrícula de conteo digital en cada sección para calcular los puntos de intersección que caen en cada tipo de tejido (hueso lamelar, hueso entrelazado, matriz osteoide, biomaterial y espacios medulares), y los porcentajes de fracción de volumen se obtuvieron mediante la relación entre los puntos de intersección que caen en cada tipo de tejido y el total de puntos de intersección de la cuadrícula.
Análisis Estadístico
No se calculó el tamaño de la muestra. Se decidió reclutar a 30 pacientes, ya que este número estaba dentro de la capacidad de los grupos de investigación presentes. Se crearon tres listas de aleatorización en línea en el sitio web del Generador de Secuencias Aleatorias (https://www.random.org). Solo uno de los investigadores (FMC), que no estaba involucrado en la selección y tratamiento de los pacientes, conocía la secuencia aleatoria y podía acceder a las listas de aleatorización almacenadas en una computadora portátil protegida por contraseña. Los códigos aleatorios se encerraron en sobres sellados, idénticos, opacos y numerados secuencialmente. Los sobres se abrieron secuencialmente después de que los pacientes elegibles firmaron el consentimiento informado; por lo tanto, la asignación del tratamiento se mantuvo oculta para los investigadores a cargo de inscribir y tratar a los pacientes. Debido a la naturaleza del estudio, después de la asignación de grupos, los cirujanos no estaban cegados. Sin embargo, las muestras fueron anonimizadas y el laboratorio de histología estuvo cegado durante los análisis.
Todos los análisis de datos se realizaron de acuerdo con el plan de análisis preestablecido. Se realizó un análisis descriptivo utilizando la media ± desviación estándar (DE) utilizando (Numbers para Mac V. 11.0 [7030.0.94], Apple Inc., Los Altos, California, EE. UU.). Los resultados dicotómicos se compararon entre grupos utilizando. Las comparaciones entre variables continuas se realizaron utilizando una prueba t independiente. Todas las comparaciones estadísticas se llevaron a cabo al nivel de significancia de 0.05. Los pacientes se utilizaron como la unidad estadística.
Resultados
Se informa un diagrama de flujo del paciente tratado en la Figura 9. Los pacientes debían ser reclutados y tratados utilizando procedimientos similares en tres centros diferentes, y se suponía que cada centro reclutaría y trataría a 10 pacientes. Sin embargo, solo un centro reclutó a todos los pacientes planificados, mientras que los otros dos centros reclutaron a cuatro pacientes cada uno. Las razones para no incluir a 12 pacientes fueron: visitas frecuentes de control (10 pacientes) y una negativa a la regeneración ósea guiada (dos pacientes). Finalmente, 18 pacientes fueron inscritos consecutivamente en el ensayo pertenecientes a una cohorte de 30 pacientes inicialmente evaluados para elegibilidad. Ocho pacientes fueron asignados aleatoriamente al grupo A, mientras que 10 pacientes fueron asignados aleatoriamente al grupo B. De estos, seis de 18 pacientes eran hombres.
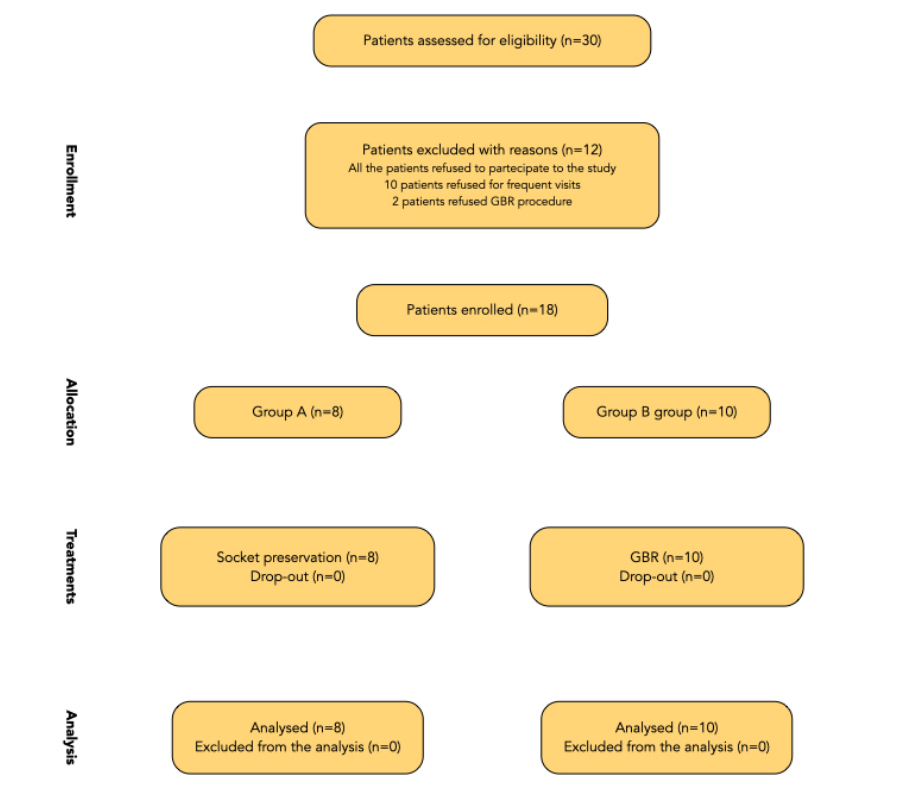
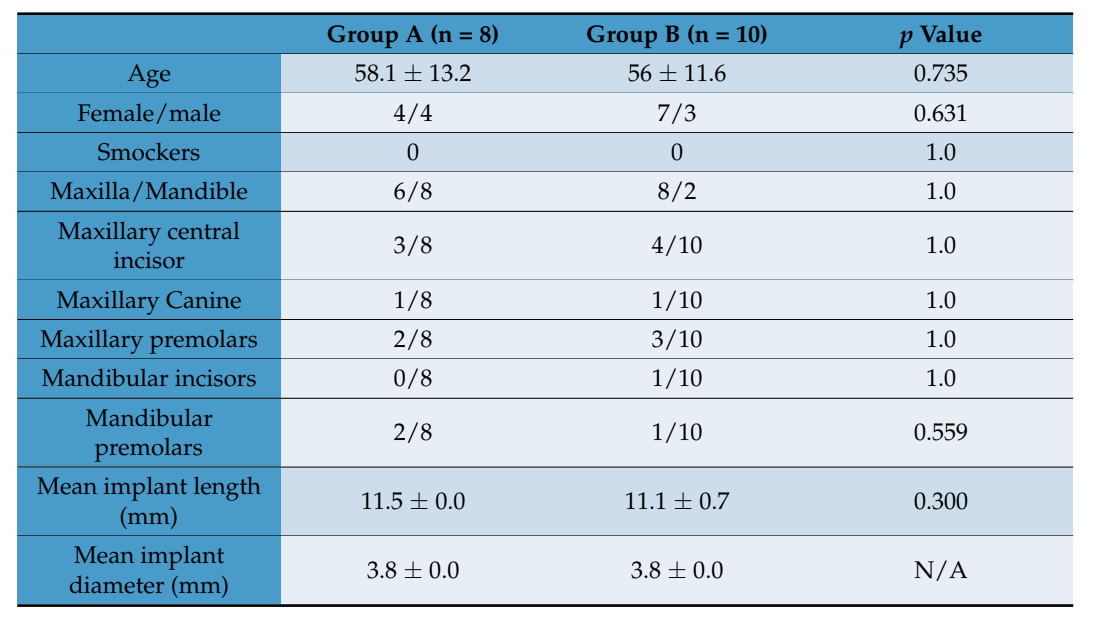
Todos los pacientes incluidos fueron tratados de acuerdo con las intervenciones asignadas. El primer paciente fue tratado en noviembre de 2018, mientras que el último tratamiento quirúrgico comenzó en septiembre de 2020. Ningún paciente abandonó el ensayo, y no se produjeron desviaciones del protocolo original; por lo tanto, todos los pacientes recibieron las coronas finales. El seguimiento medio después de la entrega de la prótesis fue de 6 a 30 meses. La edad media de los pacientes fue de 56.9 ± 11.9, ninguno de los cuales era fumador. Se colocaron dieciocho implantes, distribuidos en ocho en el grupo de prueba (preservación del alvéolo, grupo A) y 10 en el grupo de control (GBR, grupo B). Los datos de todos los pacientes incluidos fueron evaluados en los análisis estadísticos. Al comparar los grupos probados, no hay un desbalance entre ellos, incluyendo la posición y distribución de los dientes (Tabla 1).
Fallo del implante, complicaciones y satisfacción de los pacientes
No se experimentó fallo del implante ni complicaciones. Además, todos los pacientes estaban completamente satisfechos con la función y estética de su restauración soportada por implantes, y no se experimentaron diferencias en su percepción de la terapia, por lo que todos los pacientes se someterían a la misma terapia.
Análisis Histomorfométrico
El análisis morfológico no reveló signos de reacción tisular, como fibrosis o necrosis. El hueso regenerado estaba bien mineralizado en ambos grupos, pero parecía más maduro en el grupo B que en el grupo A, como se observa en la Figura 10A,B, que muestra una visión general de muestras representativas.
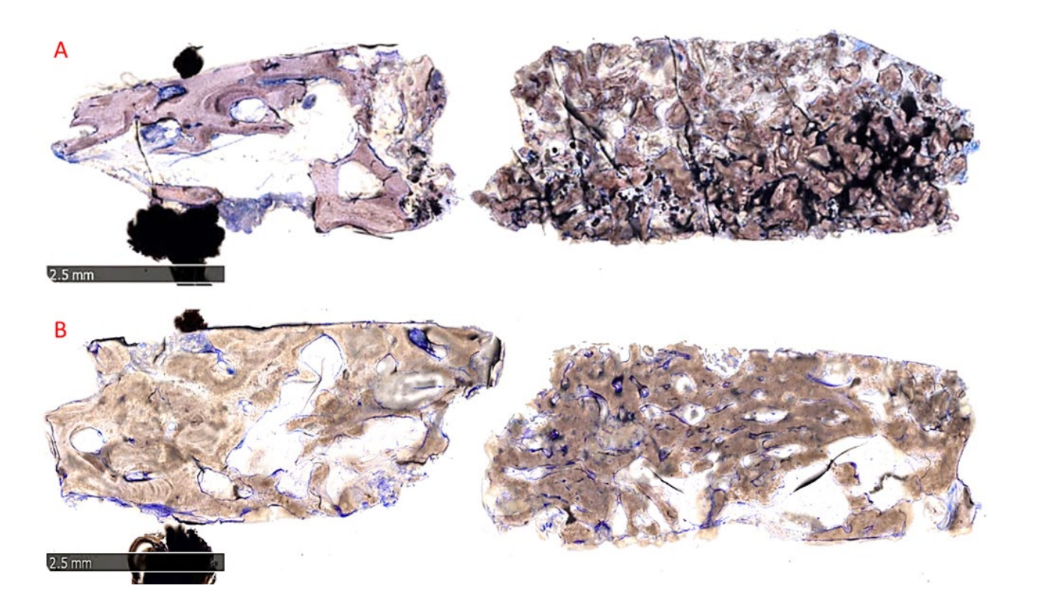
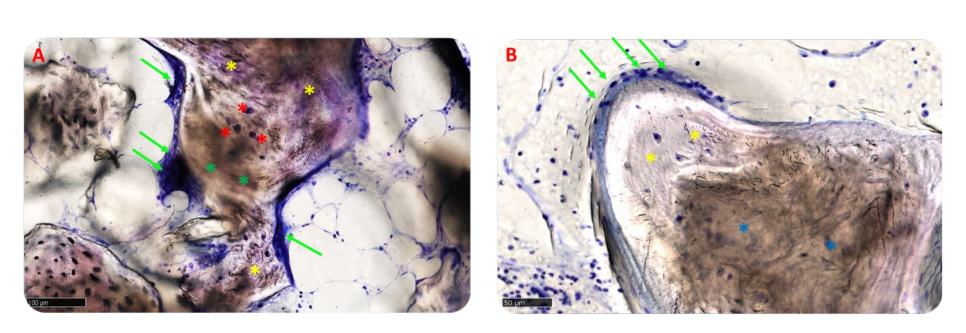
En el grupo A, las partículas injertadas estaban completamente incrustadas en la matriz ósea y parecían estar experimentando un intenso remodelado, con un grado intermedio de mineralización. No se observaron huecos en la interfaz entre los bloques residuales y el hueso recién formado (Figura 11A). En el grupo B, la matriz ósea que rodeaba las partículas del biomaterial presentaba un alto nivel de mineralización y osteointegración con un equilibrio entre la formación ósea (fase anabólica) y la degradación ósea (fase catabólica), confirmado por la presencia de algunos frentes de remodelación ósea y algunos osteoclastos (Figura 11B).
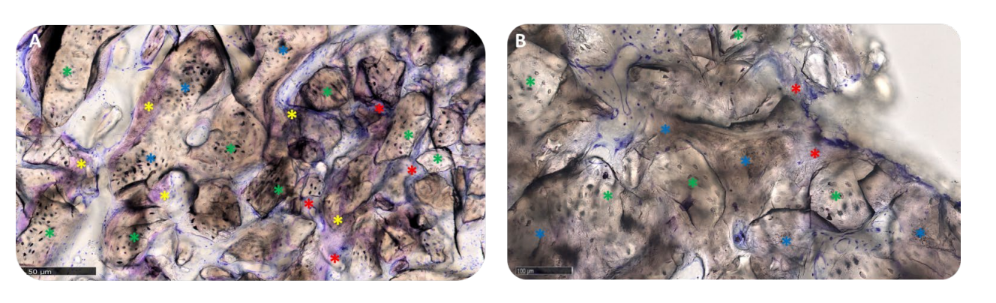
La matriz estaba en la fase anabólica activa: las áreas óseas estaban compuestas de hueso lamelar mineralizado recién formado, con osteocitos en la matriz calcificada y un frente de remodelación poblado por osteoblastos activos y pocos osteoclastos, particularmente en el grupo A (Figura 12A,B).
Tres muestras mostraron un linfocito mínimo, mientras que las muestras restantes de ambos grupos tenían solo algunas células inflamatorias dispersas (Figura 13A,B). Varios vasos sanguíneos de pequeño tamaño ocupaban los espacios medulares, donde el tejido resultó en más madurez, lo que podría indicar actividad del tejido en progreso.
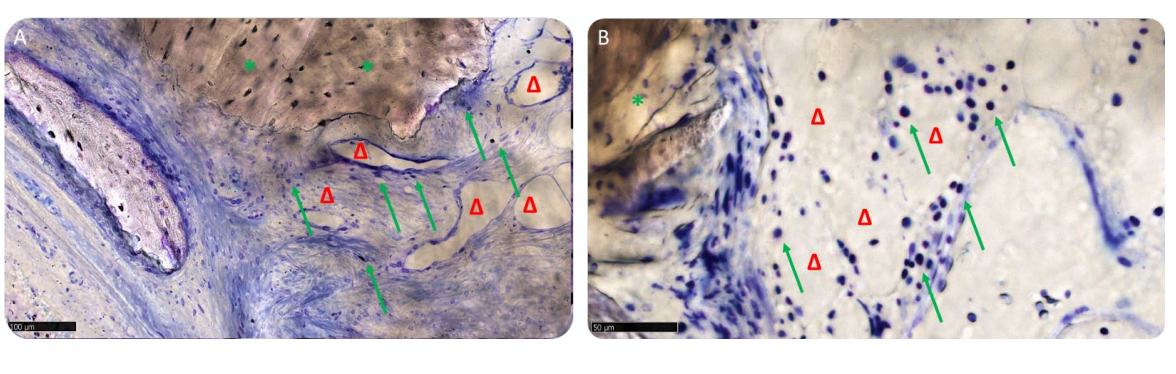
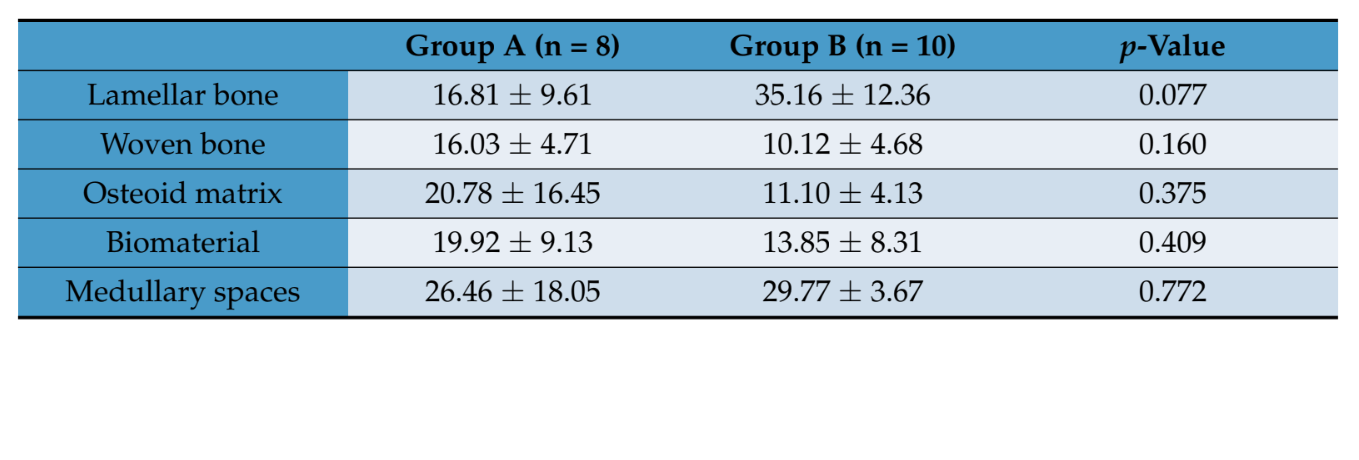
La evaluación histomorfométrica no mostró diferencias estadísticamente significativas en las fracciones de volumen de tejido entre los dos grupos de pacientes (Tabla 2). Sin embargo, en el grupo B, el hueso lamelar tuvo un valor medio más alto que el obtenido en el grupo A, donde la matriz ósea recién formada estaba representada principalmente por una matriz menos inmadura, como el osteoide y el hueso entrelazado.
Discusión
Esta investigación fue diseñada como un ensayo controlado aleatorio con el objetivo de responder a la siguiente pregunta: ¿cuál es el tratamiento sugerido para la rehabilitación del implante de los alvéolos residuales de clase II de Elian entre la membrana de politetrafluoroetileno no resorbible de alta densidad (d-PTFE) dejada intencionadamente expuesta durante 4 semanas después de la extracción dental, y la preservación del alvéolo con material óseo anorgánico, y la extracción seguida de regeneración ósea guiada, realizada dos meses después? Los resultados de la presente investigación no encontraron un tratamiento superior al otro, por lo tanto, se aceptó la hipótesis nula de que no hay diferencias estadísticamente significativas entre los dos procedimientos probados.
Aunque los resultados de la presente investigación son similares entre los grupos, el principal beneficio de la técnica de preservación del alvéolo propuesta con una membrana no resorbible puede representar una opción válida porque permite reducir el tiempo total de tratamiento y los costos para el paciente. Estos beneficios se deben principalmente a que puede reducir la necesidad de otras técnicas regenerativas, sin perjudicar los resultados finales, la previsibilidad del tratamiento con implantes, y por último, pero no menos importante, la satisfacción del paciente.
La placa bucal intacta (defecto de clase 1 de Elian) se ha considerado un requisito previo para la estabilidad de los tejidos blandos en el área que rodea el implante y, por lo tanto, para los resultados estéticos a largo plazo, particularmente en caso de altas demandas estéticas. La resorción continua de la delgada placa ósea bucal puede llevar a un alto riesgo de resorción gingival con el tiempo. El tratamiento de defectos anteriores a menudo requiere una segunda cirugía que consiste en procedimientos adicionales de regeneración ósea para permitir una inserción guiada prostéticamente de los implantes. Sin embargo, estos procedimientos generalmente no son más aceptables para los pacientes debido a su invasividad y costo. La técnica propuesta de usar una membrana no reabsorbible para reparar temporalmente la pared bucal dañada, y dejada intencionalmente expuesta por encima del alvéolo injertado, parece ser prometedora y directa, requiriendo menos procedimientos quirúrgicos. En la presente investigación, no se encontraron diferencias en el examen histológico cuantitativo. De hecho, la reconstrucción de la placa bucal con una membrana no reabsorbible intencionalmente expuesta parece ser un procedimiento efectivo y fácil para regenerar una placa ósea bucal reabsorbida, reduciendo potencialmente la necesidad de regeneración ósea guiada. La técnica propuesta puede ser fuertemente aceptada por los pacientes debido a su menor invasividad.
La razón biológica para esperar de cuatro a seis semanas antes de la membrana d-PTFE es esperar hasta el final de la fase inicial de curación, antes del proceso de remodelación ósea. En esta etapa, bajo la membrana d-PTFE, es posible esperar un cierre completo de los tejidos blandos. La membrana d-PTFE puede actuar como un andamio para guiar la curación de los nuevos tejidos blandos, preservando la forma convexa de la cresta alveolar. Por el contrario, en el grupo GBR, se recomienda un período de ocho semanas antes de la recuperación completa de los tejidos blandos, según Buser y coautores.
La membrana no reabsorbible funciona como una barrera que permite la separación de los tejidos blandos del hueso durante 4 a 6 semanas, el tiempo necesario para alcanzar la estabilización del coágulo sanguíneo. La eliminación de la membrana no reabsorbible después de este período parece dar suficiente tiempo para permitir dentro del alvéolo la diferenciación de las células mesenquimatosas en osteoblastos, excluyendo los fibroblastos del colgajo gingival, y finalmente llevando a la formación y maduración de nuevo hueso. Para este propósito, es crucial que el paciente mantenga la herida quirúrgica limpia y desinfectada. Sin embargo, se dieron sugerencias similares para ambas técnicas. En comparación con la regeneración ósea guiada por etapas, la técnica presentada permite la entrega de la restauración definitiva en un tiempo más corto, mejorando potencialmente la aceptación de los pacientes y también reduciendo potencialmente el costo total.
En un estudio histológico en humanos, se tomó una biopsia después de 4 semanas en el momento de la extracción de la membrana. Los resultados de esta investigación histológica demostraron que, incluso si la membrana d-PTFE no resorbible se dejó intencionalmente expuesta, no se encontró tejido epitelial sobre una matriz de tejido conectivo denso. Este hallazgo puede indicar que el tejido conectivo recién formado parece ser una matriz osteoide bien vascularizada. Sin embargo, necesita más tiempo para completar su maduración y convertirse en un tejido mineralizado, lo que permite la colocación del implante. Se necesita un período general de 3 a 5 meses. Básicamente, depende del tipo y tamaño del defecto y del biomaterial utilizado para injertar el alvéolo. En otro estudio histológico, el grupo de prueba recibió una combinación de 70% de material de aloinjerto cortical mineralizado y 30% de material de aloinjerto cortical desmineralizado, utilizado para injertar un alvéolo post-extracción cubierto con una membrana d-PTFE no resorbible intencionalmente expuesta. Los resultados obtenidos se evaluaron sitio por sitio con un grupo de control, para el cual solo se utilizó material de aloinjerto mineralizado. Las biopsias demostraron un aumento en la formación de hueso vital (36.16%) con una reducción consecuente del injerto residual (18.24%) en el grupo de prueba, en comparación con los casos controlados, con un 100% del grupo de aloinjerto de hueso mineralizado (24.69% y 27.04%, respectivamente).
Los resultados del presente estudio están de acuerdo con una reciente revisión sistemática de Cochrane que concluyó que las técnicas de preservación del reborde alveolar pueden minimizar los cambios generales en la altura y el ancho del reborde residual después de la extracción de dientes. Sin embargo, la evidencia es muy incierta.
Debido a la falta de cálculo del tamaño de la muestra, la principal limitación del presente estudio fue el tamaño de muestra reducido. Otra limitación, que puede alterar la validez interna y externa de los resultados, fue la falta de calibración del cirujano. Sin embargo, todos los cirujanos involucrados en esta investigación fueron capacitados para realizar dos casos explicativos antes de comenzar el ensayo. Finalmente, el maxilar y la mandíbula tienen diferentes tasas y patrones de reabsorción ósea, lo que puede afectar el pronóstico. Sin embargo, la aleatorización permitió tener dos grupos equilibrados, sin diferencias estadísticas entre ellos. Por lo tanto, los resultados del presente informe preliminar proporcionan datos histológicos cuantitativos de hueso reconstruido con membrana d-PTFE no reabsorbible, o regeneración ósea guiada para el tratamiento de defectos óseos alveolares post-extracción, con restauraciones soportadas por implantes. Aunque la técnica de curación de heridas abiertas propuesta se ha comparado con la reconstrucción ósea guiada clásica, estos resultados preliminares alientan este enfoque. Asimismo, hay estudios que comparan matriz dérmica celular vs. membrana de politetrafluoroetileno (PTFE), alcanzando resultados prometedores similares. Por lo tanto, se necesitan más estudios clínicos y radiológicos, con un seguimiento más prolongado, para validar estos prometedores resultados clínicos.
Conclusiones
Con la limitación del presente estudio piloto, la reconstrucción de la placa bucal con una membrana no reabsorbible intencionalmente expuesta parece ser un procedimiento efectivo y fácil para regenerar una placa ósea bucal reabsorbida, reduciendo la necesidad de regeneración ósea guiada. Se necesitan más estudios con un tamaño de muestra mayor para confirmar este resultado preliminar.
Roberto Luongo, Marco Tallarico, Elena Canciani, Daniele Graziano, Claudia Dellavia, Marco Gargari, Francesco Mattia Ceruso, Dario Melodia y Luigi Canullo
Referencias
- Marcus, S.; Drury, T.; Brown, L.; Zion, G. Retención dental y pérdida de dientes en la dentición permanente de adultos: Estados Unidos, 1988–1991. J. Dent. Res. 1996, 75, 684–695.
- Mecall, A.R.; Rosenfeld, A.L. Influencia de los patrones de reabsorción de crestas residuales en la colocación de implantes y la posición dental. Int. J. Periodontics Restor. Dent. 1991, 11, 8–23.
- Van der Weijden, F.; Dell’Acqua, F.; Slot, D.E. Cambios dimensionales del hueso alveolar en los alvéolos post-extracción en humanos: Una revisión sistemática. J. Clin. Periodontol. 2009, 36, 1048–1058.
- Meloni, S.M.; Jovanovic, S.A.; Pisano, M.; De Riu, G.; Baldoni, E.; Tallarico, M. Regeneración ósea guiada horizontal en una sola etapa con hueso autólogo, hueso bovino anorgánico y membranas de colágeno: Seguimiento de un estudio prospectivo 30 meses después de la carga. Eur. J. Oral Implant. 2018, 11, 89–95.
- Kan, J.Y.K.; Rungcharassaeng, K.; Lozada, J.L.; Zimmerman, G. Estabilidad del tejido gingival facial tras la colocación inmediata y provisionalización de implantes individuales anteriores maxilares: Un seguimiento de 2 a 8 años. Int. J. Oral Maxillofac. Implant. 2011, 26, 179–187.
- Zubillaga, G.; Von Hagen, S.; Simon, B.I.; Deasy, M.J. Cambios en la altura y ancho del hueso alveolar tras la augmentación de cresta post-extracción utilizando una membrana bioabsorbible fija y un injerto óseo osteoinductivo de hueso desmineralizado liofilizado. J. Periodontol. 2003, 74, 965–975.
- Darby, I.; Chen, S.T.; Buser, D. Técnicas de preservación de crestas para terapia de implantes. Int. J. Oral Maxillofac. Implant. 2009, 24, 260–271.
- Tallarico, M.; Xhanari, E.; Pisano, M.; Gatti, F.; Meloni, S.M. Reemplazo de molares con implantes de 7 mm de diámetro: ¿Colocar el implante inmediatamente o esperar 4 meses después de la preservación del alvéolo? Resultados de un ensayo controlado aleatorio 1 año después de la carga. Eur. J. Oral Implant. 2017, 10, 169–178.
- Canullo, L.; Marin, G.W.; Tallarico, M.; Canciani, E.; Musto, F.; Dellavia, C. Evaluación histológica e histomorfométrica de sitios post-extractivos injertados con nano-hidroxiapatita enriquecida con Mg: Un ensayo controlado aleatorio comparando 4 versus 12 meses de cicatrización. Clin. Implant. Dent. Relat. Res. 2015, 18, 973–983.
- Meloni, S.M.; Tallarico, M.; Lolli, F.M.; Deledda, A.; Pisano, M.; Jovanovic, S.A. Preservación del alvéolo post-extracción utilizando injerto de tejido conectivo epitelial versus matriz de colágeno porcino. Resultados de un ensayo controlado aleatorio a un año. Eur. J. Oral Implant. 2015, 8, 39–48.
- Papi, P.; Di Murro, B.; Tromba, M.; Passarelli, P.C.; D’Addona, A.; Pompa, G. El uso de una membrana no absorbible como barrera oclusiva para la preservación de la cresta alveolar: Un estudio prospectivo de seguimiento de un año. Antibiotics 2020, 9, 110.
- Sun, D.-J.; Lim, H.-C.; Lee, D.-W. Preservación de la cresta alveolar utilizando un enfoque de membrana abierta para alvéolos con deficiencia ósea: Un ensayo clínico controlado aleatorio. Clin. Implant Dent. Relat. Res. 2018, 21, 175–182.
- Chatzopoulos, G.S.; Koidou, V.P.; Sonnenberger, M.; Johnson, D.; Chu, H.; Wolff, L.F. Preservación de la cresta post-extracción utilizando membranas de PTFE densas: Una revisión sistemática y metaanálisis. J. Prosthet. Dent. 2022.
- Carbonell, J.M.; Martin, I.S.; Santos, A.; Pujol, A.; Sanz-Moliner, J.D.; Nart, J. Membranas de politetrafluoroetileno de alta densidad en procedimientos de regeneración ósea y de tejidos guiados: Una revisión de la literatura. Int. J. Oral Maxillofac. Surg. 2014, 43, 75–84.
- Atieh, M.A.; Alsabeeha, N.H.M.; Payne, A.G.T.; Duncan, W.; Faggion, C.M.; Esposito, M. Intervenciones para reemplazar dientes perdidos: Técnicas de preservación de crestas alveolares para el desarrollo de sitios de implantes dentales. Cochrane Database Syst. Rev. 2021, CD010176.
- Corbella, S.; Taschieri, S.; Francetti, L.; Weinstein, R.; Del Fabbro, M. Resultados histomorfométricos tras la cicatrización del alvéolo post-extracción con diferentes biomateriales: Una revisión sistemática de la literatura y metaanálisis. Int. J. Oral Maxillofac. Implant. 2017, 32, 1001–1017.
- Elian, N.; Cho, S.-C.; Froum, S.; Smith, R.B.; Tarnow, D.P. Una clasificación simplificada de alvéolos y técnica de reparación. Pract. Proced. Aesthetic Dent. 2007, 19, 99–104.
- Buser, D.; Chappuis, V.; Belser, U.C.; Chen, S. Colocación de implantes post-extracción en sitios estéticos de un solo diente: ¿Cuándo inmediato, cuándo temprano, cuándo tarde? Periodontology 2000 2017, 73, 84–102.
- Canciani, E.; Ragone, V.; Biffi, C.A.; Valenza, F.; D’Ambrosi, R.; Olimpo, M.; Cristofalo, A.; Galliera, E.; Dellavia, C. Comprendiendo el papel de la modificación de la superficie de estructuras de titanio trabecular aleatorias en la regeneración del tejido óseo: Un estudio experimental. Medicina 2022, 58, 315.
- Kan, J.Y.K.; Rungcharassaeng, K.; Lozada, J.L. Colocación inmediata y provisionalización de implantes individuales anteriores maxilares: Estudio prospectivo de 1 año. Int. J. Oral Maxillofac. Implant. 2003, 18, 31–39.
- Bambini, F.; Orilisi, G.; Quaranta, A.; Memè, L. Carga inmediata biológicamente orientada: Un nuevo protocolo matemático de inserción vertical de implantes, estudio de seguimiento de cinco años. Materials 2021, 14, 387.
- Chen, S.T.; Buser, D. Resultados estéticos tras la colocación inmediata y temprana de implantes en el maxilar anterior: Una revisión sistemática. Int. J. Oral Maxillofac. Implant. 2014, 29, 186–215.
- Bartee, B.K. Una técnica simplificada para la preservación de crestas tras la extracción dental. Dent. Today 1995, 14, 62–67.
- Laurito, D.; Cugnetto, R.; Lollobrigida, M.; Guerra, F.; Vestri, A.; Gianno, F.; Bosco, S.; Lamazza, L.; De Biase, A. Preservación del alvéolo con membrana d-PTFE: Análisis histológico de la matriz recién formada en la extracción de la membrana. Int. J. Periodontics Restor. Dent. 2016, 36, 877–883.
- Beck, T.M.; Mealey, B.L. Análisis histológico de la cicatrización tras la extracción dental con preservación de cresta utilizando aloinjerto de hueso humano mineralizado. J. Periodontol. 2010, 81, 1765–1772.
- Borg, T.D.; Mealey, B.L. Cicatrización histológica tras la extracción dental con preservación de cresta utilizando aloinjerto de hueso mineralizado versus combinado mineralizado-desmineralizado liofilizado: Un ensayo clínico controlado aleatorio. J. Periodontol. 2015, 86, 348–355.
- Krauser, J.T. Membranas de PTFE de alta densidad: Usos con implantes de forma radicular. Dent. Implant. Update 1996, 7, 65–69.
- Fotek, P.D.; Neiva, R.F.; Wang, H.-L. Comparación de matriz dérmica y membrana de politetrafluoroetileno para la augmentación ósea del alvéolo: Un estudio clínico e histológico. J. Periodontol. 2009, 80, 776–785.