Mallas de titanio ultra finas semi-personalizadas en la regeneración ósea guiada para terapia de implantes en defectos alveolares severos: un informe de caso
Traducción automática
El artículo original está escrito en idioma EN (enlace para leerlo) .
Resumen
Este informe de caso proporciona una descripción detallada de un procedimiento de regeneración ósea simple y rápido utilizando una malla de titanio ultra fina semipersonalizada en tres dimensiones. Un hombre de 50 años con un defecto óseo vertical y horizontal severo en la mandíbula anterior se sometió a un tratamiento de implante en un enfoque por etapas. El hueso autólogo se combinó con un xenoinjerto, y la mezcla se injertó para aumentar el defecto óseo y se cubrió con mallas de titanio ultra finas semipersonalizadas, que se seleccionaron entre sus varios tipos según el tamaño y la configuración del defecto óseo, conectadas directamente e inmovilizadas en los tornillos de soporte con un modelado mínimo. En una cirugía de reingreso postoperatorio de 6 meses, se retiraron las mallas de titanio realizadas, se colocaron los implantes y se obtuvo una biopsia de núcleo óseo que demostró una formación ósea nueva satisfactoria. Finalmente, dos meses después, se instaló la prótesis definitiva. Esta malla de titanio ultra fina semipersonalizada podría ayudar a un clínico de implantes a obtener resultados más predecibles en la regeneración ósea guiada (GBR).
Antecedentes
La regeneración ósea guiada (GBR) es una técnica utilizada para aumentar la falta de hueso alveolar horizontal y/o vertical. Existen varios principios importantes para el éxito de la GBR, incluyendo la exclusión del tejido epitelial, el mantenimiento del espacio de injerto, la estabilización de un coágulo de fibrina y la curación sin interrupciones mediante un cierre de herida sin tensión. Para lograr esos principios, se deben incorporar membranas de barrera reabsorbibles o no reabsorbibles en los procedimientos de GBR. Una membrana de colágeno reabsorbible es fácil de manipular y no requiere cirugía adicional para su extracción, pero es difícil predecir el tiempo exacto de degradación o reabsorción y mantener un espacio de injerto más grande sin colapsar. Por el contrario, una membrana no reabsorbible requiere cirugía adicional para su extracción, pero generalmente muestra un mejor resultado de regeneración ósea, a menos que la curación se interrumpa por exposición.
La malla de titanio es un tipo representativo de membrana no reabsorbible que se caracteriza por su rigidez inherente y produce una regeneración ósea satisfactoria en defectos grandes. Sin embargo, la regeneración ósea con malla de titanio podría complicarse por exposición, que frecuentemente resulta de puntos y ángulos afilados de su corte, doblado y recorte para ajustar la malla de titanio a la cobertura del hueso injertado. Además, tales injertos son vulnerables a infecciones postoperatorias. El término “semi-personalizado” se utiliza en este estudio ya que las mallas de titanio no están completamente personalizadas utilizando CAD/CAM. En su lugar, el clínico podría seleccionar de una gama de mallas estándar que estaban disponibles en diferentes tamaños y configuraciones para los defectos óseos de cada paciente. En este informe de caso, describimos un procedimiento de GBR simple y rápido que utiliza mallas de titanio ultra-finas semi-personalizadas para su aplicación en un gran defecto óseo.
Presentación del caso
Pacientes y procedimiento quirúrgico
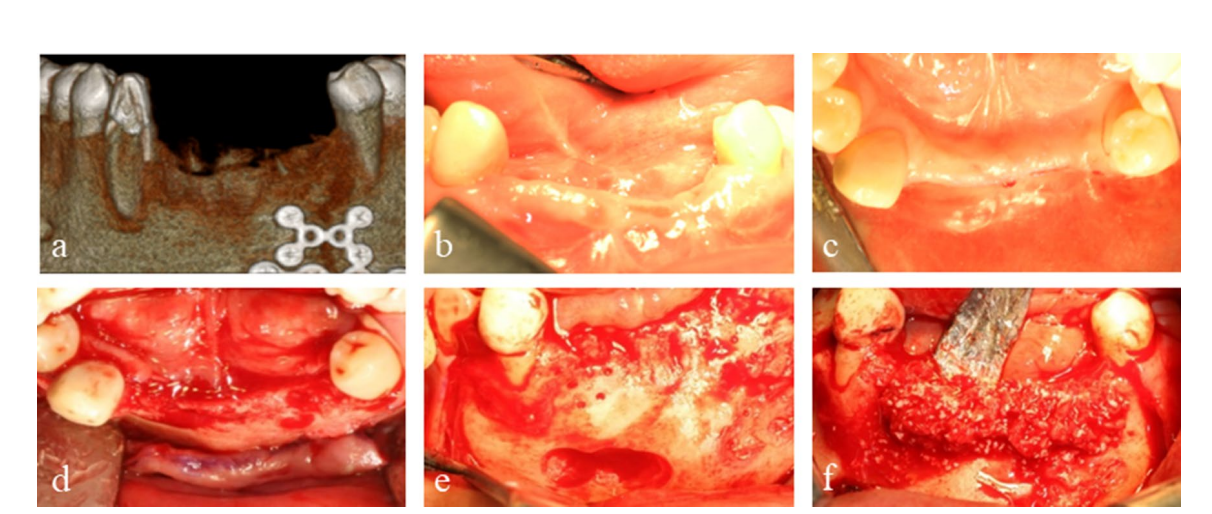
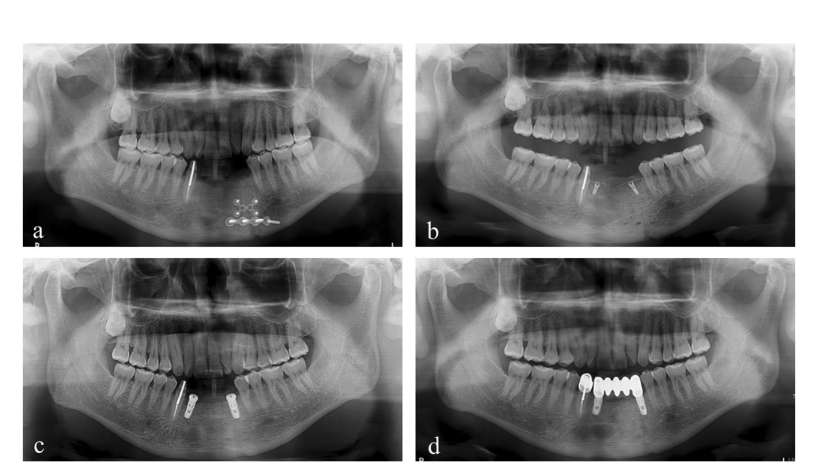
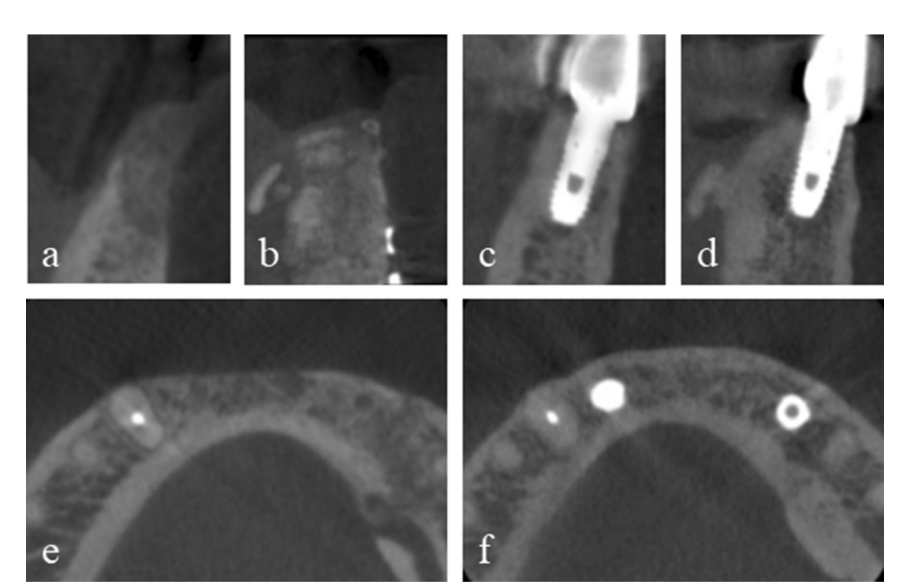
Un hombre de 50 años con un defecto óseo alveolar combinado vertical y horizontal en la mandíbula anterior debido a un trauma facial previo, fue referido para tratamiento con implantes. Su historial médico incluía reducción abierta y fijación interna de una fractura mandibular compuesta resultante de un accidente de tráfico. El incisivo lateral mandibular izquierdo y el canino fueron avulsionados con la fractura del hueso alveolar y el incisivo central mandibular izquierdo y el incisivo central y lateral mandibular derecho fueron extraídos durante la cirugía de fractura. Una fractura de corona del canino mandibular derecho fue restaurada con un poste y núcleo después de un tratamiento de conducto radicular. En la evaluación preoperatoria de tomografía computarizada de haz cónico (CBCT), el defecto del área mandibular anterior se midió en aproximadamente 7 mm verticalmente y 5 mm horizontalmente (Fig. 1a).
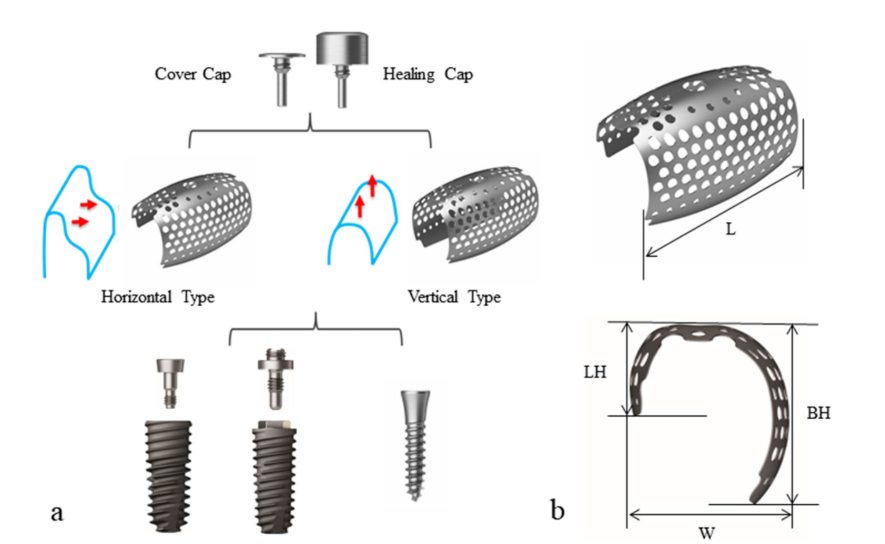
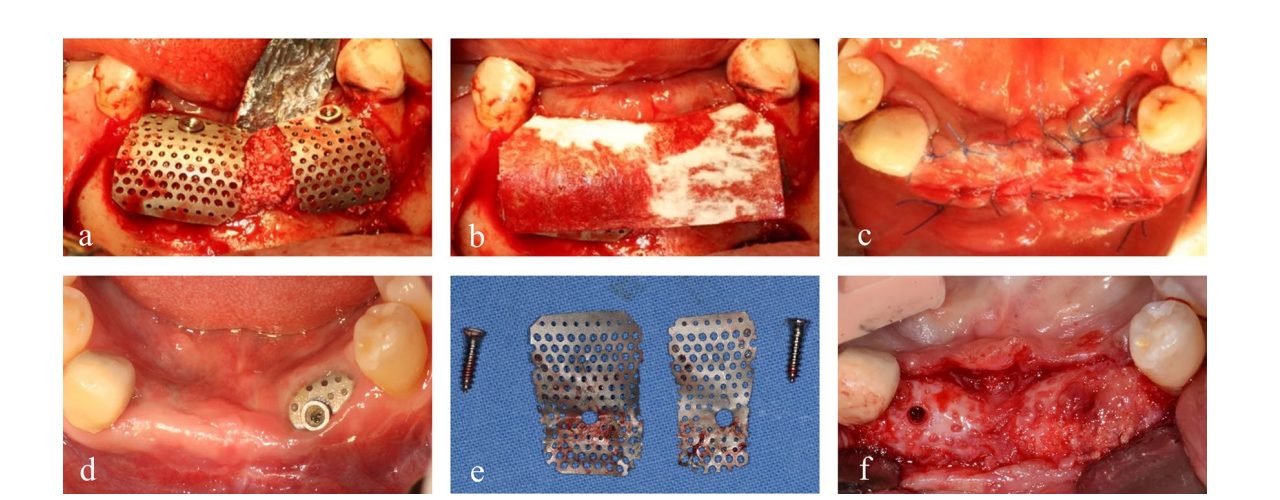
El paciente proporcionó su consentimiento informado, y se llevó a cabo una augmentación ósea en etapas para la colocación del implante. Después de la infiltración de lidocaína al 2% con 1:100,000 de epinefrina, se realizó una incisión media crestal con dos incisiones verticales desde el primer premolar mandibular izquierdo hasta el primer premolar derecho, y se reflejó un colgajo mucoperióstico de grosor completo. Se retiraron las placas y tornillos de la cirugía de fractura anterior. Se insertaron dos tornillos de tensión en las posiciones óptimas de los implantes posteriores, y se confirmó clínicamente y se midió cuidadosamente el tamaño y la configuración del defecto óseo, que había sido evaluado preoperatoriamente por CBCT. El hueso autólogo, que se cosechó de la ubicación de las placas y tornillos y se particuló con un taladro trepanador especializado (colector de autobone, Osstem, República de Corea), se mezcló con un xenoinjerto (A-Oss, Osstem) en una proporción de volumen 1:1 y se injertó para aumentar el defecto óseo vertical y horizontal alrededor de los tornillos de tensión (Fig. 1b–f). Se eligieron específicamente dos mallas de titanio ultra-finas semi-personalizadas (OssBuilder, Osstem), como tipo horizontal con dimensiones de longitud 10 mm, ancho 9 mm, altura bucal 11 mm y altura lingual 5.5 mm, de varios subconjuntos disponibles (Fig. 2). Estas mallas de titanio se ajustaron para cubrir el área injertada mediante cortes y modelado mínimos y se inmovilizaron con tapas de cobertura. Se colocó una membrana de colágeno reabsorbible (Oss-Mem hard, Osstem) sobre las mallas de titanio para minimizar el adelgazamiento prematuro de la encía superior. Finalmente, se realizó un cierre primario sin tensión con una incisión de liberación en el periostio bucal (Fig. 3a–c).
El paciente recibió antibióticos orales y analgésicos y se le indicó que usara una solución de gluconato de clorhexidina al 0.12% durante 10 días.
Resultados
Excepto por una pequeña exposición de la malla de titanio ultra-fina semi-personalizada en la posición del canino mandibular izquierdo, no hubo complicaciones. El tamaño de la exposición aumentó constantemente hasta aproximadamente
5 mm de diámetro. Los tejidos alrededor de la exposición eran de color rojizo pero no mostraron signos adversos ni inflamación. Seis meses después, se realizó una cirugía de reingreso bajo anestesia local y se retiraron las mallas de titanio. El examen macroscópico reveló hueso regenerado, que estaba corticalizado y revestido con un delgado pseudoperiósteo. Sin embargo, en el área donde la malla de titanio estaba expuesta, había un pseudoperiósteo más grueso, entremezclado con partículas crudas de xenoinjerto. Este pseudoperiósteo se desprendió fácilmente del hueso regenerado subyacente durante la perforación del implante (Fig. 3d–f).
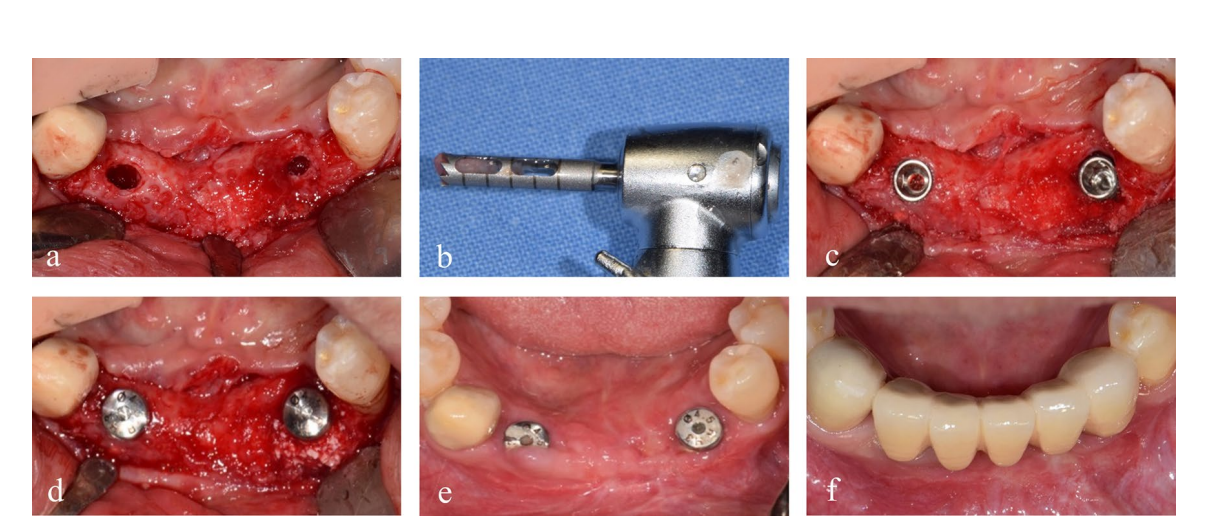
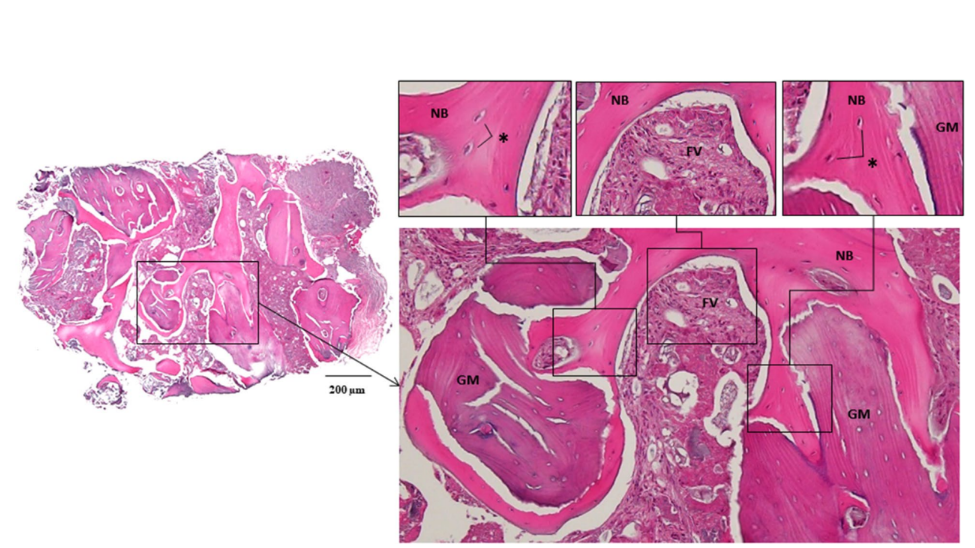
Se colocaron dos fijaciones de implante de 4.0 × 10 mm (TS III SOI, Osstem) en el hueso regenerado del canino mandibular izquierdo y el incisivo lateral derecho con un par de apriete que superó los 30 Ncm. Luego se conectaron dos pilares de cicatrización de 5.0 × 3 mm. Antes de la perforación del implante en el área correspondiente al canino mandibular izquierdo, se obtuvo un núcleo óseo para análisis histológico utilizando un taladro de trefina de 2.0 mm de diámetro (Fig. 4). Las secciones se tiñeron con hematoxilina y eosina (H&E) y se observaron utilizando un microscopio óptico (Fig. 5). Las áreas de nuevo hueso, material de injerto residual y tejidos fibrovasculares se dividieron y se midieron sus porcentajes relativos. Dos meses después, se realizaron la toma de impresiones y la entrega de la restauración definitiva de zirconia. La radiografía panorámica postoperatoria reveló un nivel óseo peri-implantario estable y, notablemente, el paciente expresó satisfacción con el resultado final (Figs. 6 & 7).
Discusión
En casos de defectos óseos horizontales y verticales severos combinados, se debe realizar un injerto óseo antes de la colocación del implante. Durante este enfoque de tratamiento paso a paso, la estabilidad del espacio de injerto óseo puede verse perturbada por eventos rutinarios en la cavidad oral, como la masticación y el habla. Por lo tanto, si un paciente requiere una cantidad sustancial de injerto óseo, la malla de titanio se considera la membrana de barrera no reabsorbible más adecuada para mantener la forma y el volumen del injerto óseo porque, al ser un metal ligero, es rígido y rentable. En comparación con los microporos de otras membranas de barrera, la malla de titanio es única en que tiene macroporos que no bloquean ni permiten el paso de células de manera selectiva. Debido a su biocompatibilidad y estabilización del coágulo sanguíneo, la malla de titanio también se ha utilizado ampliamente en el campo de la cirugía oral y maxilofacial.
Aunque es flexible y de textura suave, la malla de titanio tiene una desventaja crítica de exposición, que generalmente no es cubierta nuevamente por la encía. Se informó que la incidencia de exposición asociada con la malla de titanio varía del 16 al 34%. Su rigidez es favorable para el mantenimiento del espacio de injerto, pero con frecuencia causa adelgazamiento de la mucosa que la recubre durante la contracción de la herida en el período de curación. Además, el uso de una malla de titanio como membrana de barrera es un procedimiento muy sensible a la técnica porque debe ser moldeada y fijada rígidamente. Durante este procedimiento de moldeado, los puntos y ángulos afilados causados por el corte, doblado y recorte de la malla de titanio podrían contribuir a su exposición a través de la encía.
Diferente de una placa de malla de titanio convencional, una malla de titanio ultra-fina semi-personalizada se puede personalizar simplemente seleccionando la más adecuada entre sus varios tipos y subconjuntos de acuerdo con el tamaño y la configuración del defecto óseo. Así, se puede utilizar de manera simple y rápida porque la personalización permite una modificación mínima, eliminando puntos y ángulos afilados durante la conformación rutinaria. Generalmente, como la malla de titanio ultra-fina semi-personalizada se elige evaluando con precisión el tipo, longitud, ancho y altura del defecto óseo peri-implantario mediante una sonda periodontal o un calibrador de profundidad de implante y se conecta directamente al implante, se podría realizar un injerto óseo de manera específica y eficiente para el resultado más óptimo. Además, su fijación rígida y estabilización estable también se logran de manera fácil y rápida. Considerando que la impresión tridimensional de una malla de titanio específica para el paciente basada en un conjunto de datos CBCT preoperatorio es costosa y requiere un flujo de trabajo digital complicado, esta malla de titanio ultra-fina semi-personalizada es rentable y lista para usar, como una malla de titanio lista para usar. Si es necesario, esta malla de titanio ultra-fina semi-personalizada se puede modificar mediante un recorte y doblado mínimos para un mejor ajuste a un defecto óseo. Además, la malla de titanio y sus componentes utilizados en este caso eran versátiles, extendiendo su utilidad a implantes con conexiones internas y externas fabricadas por otros fabricantes.
La malla de titanio ultra-fina semipersonalizada tridimensional está compuesta de titanio comercialmente puro de grado 2, con un grosor de 0.1 mm. Tiene tres poros de diferentes tamaños; 1.0 mm alrededor del implante, 0.6 mm en la extensión y 0.5 mm en los lados de la malla de titanio. Con los poros de 1.0 mm, se puede proporcionar un suministro sanguíneo adecuado y difusión de factores de crecimiento para promover la curación. Los poros de 0.6 mm también permiten un suministro sanguíneo adecuado y pueden prevenir la migración del material de injerto óseo. Además, la malla de titanio ultra-fina semipersonalizada tiene poros de 0.5 mm en sus lados, que están diseñados para preservar la rigidez mecánica durante su conformación.
El hueso autólogo, el estándar de oro del material de injerto óseo debido a su efecto osteogénico, fue cosechado, particulado y utilizado en el presente caso. Se utilizó hueso cortico-canceloso para el efecto de mantenimiento de volumen del hueso cortical duro y el efecto pluripotencial del hueso esponjoso suelto. Los sitios intraorales comunes para recolectar hueso autólogo incluyen la sínfisis mandibular, la tuberosidad maxilar, el ramo, los tori o las exostosis. En nuestro caso, el sitio de operación fue el área anterior de la mandíbula, por lo tanto, el hueso autólogo fue cosechado de la sínfisis mandibular con una pequeña extensión de la reflexión del colgajo, lo que no requirió un sitio quirúrgico adicional. Reducir el número de sitios quirúrgicos tiene las ventajas de una recuperación rápida y menos complicaciones. Además, un xenoinjerto bovino, que mostró poca o ninguna resorción durante la osteoconducción, se mezcló con el hueso autólogo. En el análisis histomorfométrico, la eliminación de las mallas de titanio ultra-finas semipersonalizadas reveló una regeneración ósea exitosa revestida con un delgado pseudoperiósteo. Histológicamente, se midió que estaba compuesto por un 36.6% de hueso nuevo, un 36.0% de material de injerto residual y un 27.4% de tejido fibrovascular en la reentrada (Fig. 5).
Sin embargo, en el área de exposición de la malla de titanio, el pseudoperiósteo era mucho más grueso, y la calidad del hueso regenerado subyacente era tan pobre que el hueso regenerado no pudo resistir la perforación del implante y se rompió, siendo necesario un injerto xenogénico adicional para cubrir los dos hilos expuestos de la parte superior del implante. Un estudio previo también mostró que era posible dejar la malla de titanio en su lugar después de la exposición, aunque se encontró menos hueso regenerativo en el área expuesta. La aplicación de una membrana de colágeno reabsorbible sobre la malla de titanio, como en este caso, es actualmente controvertida. Nuestro propósito era promover la oclusividad celular y prevenir el adelgazamiento prematuro de la encía superior creando una clara separación entre los compartimentos para la regeneración ósea y epitelial.
Conclusión
En conclusión, el presente caso demostró que la GBR se puede realizar de manera simple y rápida con una malla de titanio ultra-fina semi-personalizada. La malla de titanio ultra-fina semi-personalizada debe ser seleccionada adecuadamente según el tamaño y la configuración del defecto óseo y luego conectada e inmovilizada al fixture del implante o tornillo de soporte. Esta malla de titanio ultra-fina semi-personalizada podría ayudar a un clínico de implantes a obtener resultados más predecibles en la GBR para defectos severos de hueso alveolar horizontal y vertical.
Dae‑Ho Park, Jong‑Hun Jun, Seo‑Hyoung Yun, Baek‑Sun Choi, Joseph P. Fiorellini, Marco Tallarico, Kyung‑Gyun Hwang y Chang‑Joo Park
Referencias
- Liu J, Kerns DG. Supl 1: mecanismos de regeneración ósea guiada: una revisión. Open Dent J. 2014;8:56.
- Wang H‑L, Boyapati L. Principios “PASS” para una regeneración ósea predecible. Implant Dent. 2006;15(1):8–17.
- Dahlin C, Linde A, Gottlow J, Nyman S. Curación de defectos óseos mediante regeneración de tejidos guiada. Plast Reconstr Surg. 1988;81(5):672–6.
- Dahlin C, Sennerby L, Lekholm U, Linde A, Nyman S. Generación de nuevo hueso alrededor de implantes de titanio utilizando una técnica de membrana: un estudio experimental en conejos. Int J Oral Maxillofac Implants. 1989;4(1):19–25.
- Becker W. Regeneración de tejidos guiada para implantes colocados en alvéolos de extracción y para dehiscencias de implantes: técnicas quirúrgicas e informes de casos. Int J Periodont Rest Dent. 1990;10:377–91.
- Becker W. Formación ósea en sitios de implantes dentales dehiscentes tratados con material de aumento de implante: un estudio piloto en perros. Int J Periodont Rest Dent. 1990;10:93–101.
- Rakhmatia YD, Ayukawa Y, Furuhashi A, Koyano K. Membranas de barrera actuales: malla de titanio y otras membranas para regeneración ósea guiada en aplicaciones dentales. J Prosthodont Res. 2013;57(1):3–14.
- Tallarico M, Ceruso FM, Muzzi L, Meloni SM, Kim Y‑J, Gargari M, et al. Efecto de la colocación inmediata de implantes y la reconstrucción ósea guiada con membranas de malla de titanio ultrafina en parámetros radiográficos y clínicos después de 18 meses de carga. Materials. 2019;12(10):1710.
- Jovanovic SA, Nevins M. Formación ósea utilizando membranas de barrera reforzadas con titanio. Int J Periodontics Restorative Dent. 1995;15(1):56–69.
- Malchiodi L, Scarano A, Quaranta M, Piattelli A. Fijación rígida mediante malla de titanio en la expansión de crestas edéntulas para aumento horizontal de cresta en el maxilar. Int J Oral Maxillofac Implants. 1998;13(5):701–5.
- Barboza E, Caúla A, Machado F. Potencial de la proteína morfogenética ósea humana recombinante‑2 en la regeneración ósea. Implant Dent. 1999;8(4):360–7.
- dal Polo MR, Poli PP, Rancitelli D, Beretta M, Maiorana C. Reconstrucción de crestas alveolares con mallas de titanio: una revisión sistemática de la literatura. Med Oral Patol Oral Cir Bucal. 2014;19(6): e639.
- Hartmann A, Seiler M. Minimización del riesgo de exposiciones de mallas de titanio personalizadas: un análisis retrospectivo. BMC Oral Health. 2020;20(1):1–9.
- Wang EA, Rosen V, D’Alessandro JS, Bauduy M, Cordes P, Harada T, et al. La proteína morfogenética ósea humana recombinante induce formación ósea. Proc Natl Acad Sci. 1990;87(6):2220–4.
- Toriumi DM, Kotler HS, Luxenberg DP, Holtrop ME, Wang EA. Reconstrucción mandibular con un factor inductivo de hueso recombinante: evaluación funcional, histológica y biomecánica. Arch Otolaryngol‑Head Neck Surg. 1991;117(10):1101–12.
- de Faria ABC, Chiantia FB, Teixeira ML, Aloise AC, Pelegrine AA. Estudio comparativo entre células madre mesenquimatosas derivadas de médula ósea y de tejido adiposo, asociadas con injerto xenogénico, en reconstrucciones appositivas: estudio histomorfométrico en calvaria de conejo. Int J Oral Maxillofac Implants. 2016;31(6):e155–61.
- Proussaefs P. Evaluación clínica e histológica del uso de toros mandibulares como sitio donante para autoinjertos en bloque mandibulares: informe de tres casos. Int J Periodontics Restorative Dent. 2006;26(1):43–51.
- Her S, Kang T, Fien MJ. Malla de titanio como alternativa a una membrana para aumento de cresta. J Oral Maxillofac Surg. 2012;70(4):803–10.
- Lim J, Jun SH, Tallarico M, Park JB, Park DH, Hwang KG, Park CJ. Un ensayo controlado aleatorio de regeneración ósea guiada para defectos de dehiscencia peri-implantaria con dos materiales de hueso bovino anorgánico cubiertos por mallas de titanio. Materials. 2022;15(15):5294.
