Manejo de la Enfermedad Endodóntica Refractaria con Limpieza Apical Radial
Traducción automática
El artículo original está escrito en idioma EN (enlace para leerlo) .
Introducción
Uno de los atributos definitorios de un astuto endodoncista es la capacidad de tratar con éxito la enfermedad endodóntica refractaria. La enfermedad refractaria se define como una enfermedad que es recalcitrante, no receptiva, obstinada, ingobernable o resistente al tratamiento o cura. Si bien la patogénesis de la enfermedad endodóntica refractaria no se comprende claramente, es muy probable que las influencias microbiológicas y del sistema inmunológico del huésped jueguen un papel importante. Los resultados endodónticos no exitosos a menudo se atribuyen a infecciones persistentes perpetuadas por bacterias atrapadas o por reinfección de un sistema de conducto radicular previamente desinfectado, comúnmente a través de filtraciones coronales o fracturas dentales. Las causas extra-radiculares son menos comunes e incluyen actinomicosis periapical, cristales de colesterol, reacciones a cuerpos extraños, lesiones quísticas no resueltas y biofilm extra-radicular, y generalmente requieren intervención quirúrgica o extracción del diente.
Enfermedad Endodóntica Refractaria
A continuación se presenta un ejemplo de un caso clínico (Fig. 1). Fue publicado en línea por un endodoncista y se presenta con su autorización. Involucra el retratamiento de un primer molar inferior derecho con un diagnóstico de periodontitis apical sintomática. Las mediciones de sondaje periodontal eran normales sin evidencia de fractura dental. Se tomó un CBCT, pero no se publicó. El tratamiento siguió un protocolo endodóntico estándar con aplicación a largo plazo de hidróxido de calcio que se reaplicó dos veces durante un período de siete meses. A medida que los síntomas del paciente mejoraron algo, los conductos fueron obturados y el diente restaurado. ¡Una semana después, el diente fue extraído debido a la persistencia de los síntomas!
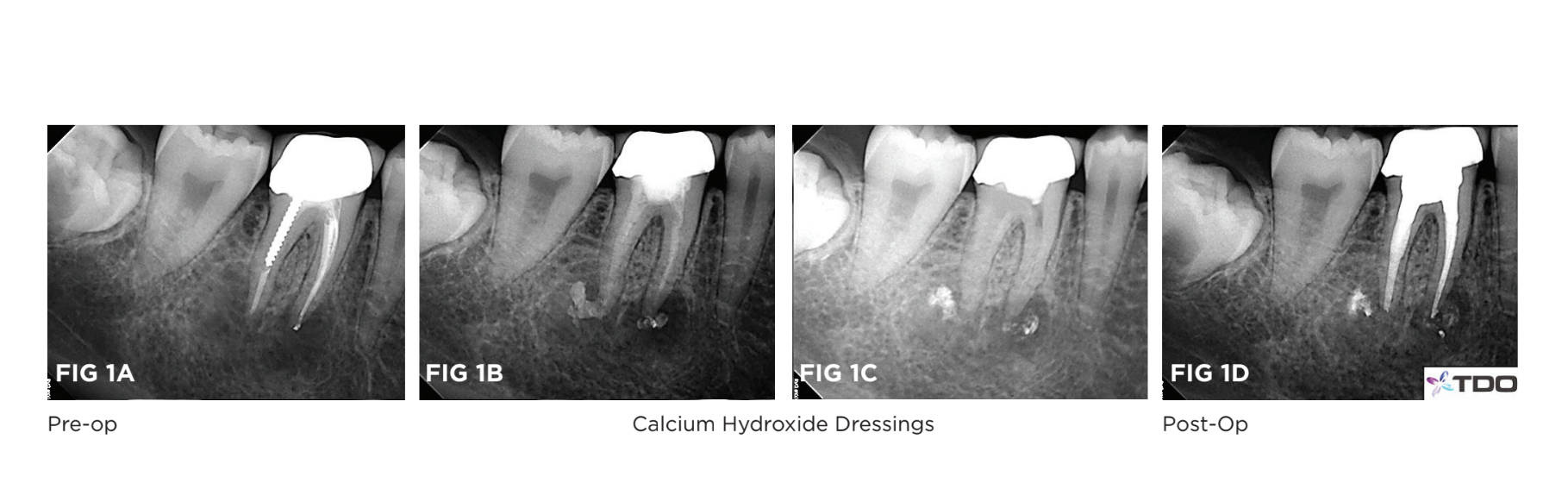
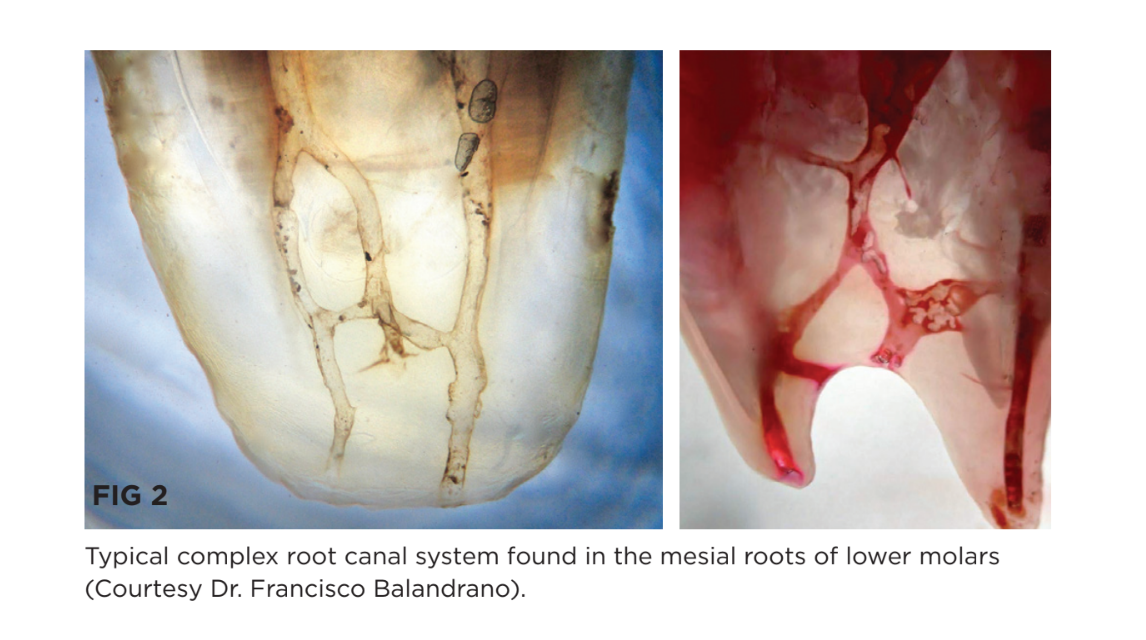
Aunque la etiología del tratamiento fallido y la incapacidad para resolver los síntomas nunca se determinó, una fuerte posibilidad es que el protocolo utilizado fue ineficaz para reducir suficientemente la carga biológica dentro del diente. Se sabe que los molares inferiores tienen un sistema de conductos radiculares complicado, especialmente en la raíz mesial (Fig. 2) y las técnicas actuales de instrumentación e irrigación no logran abordar adecuadamente esta anatomía.
Informe de Caso #1
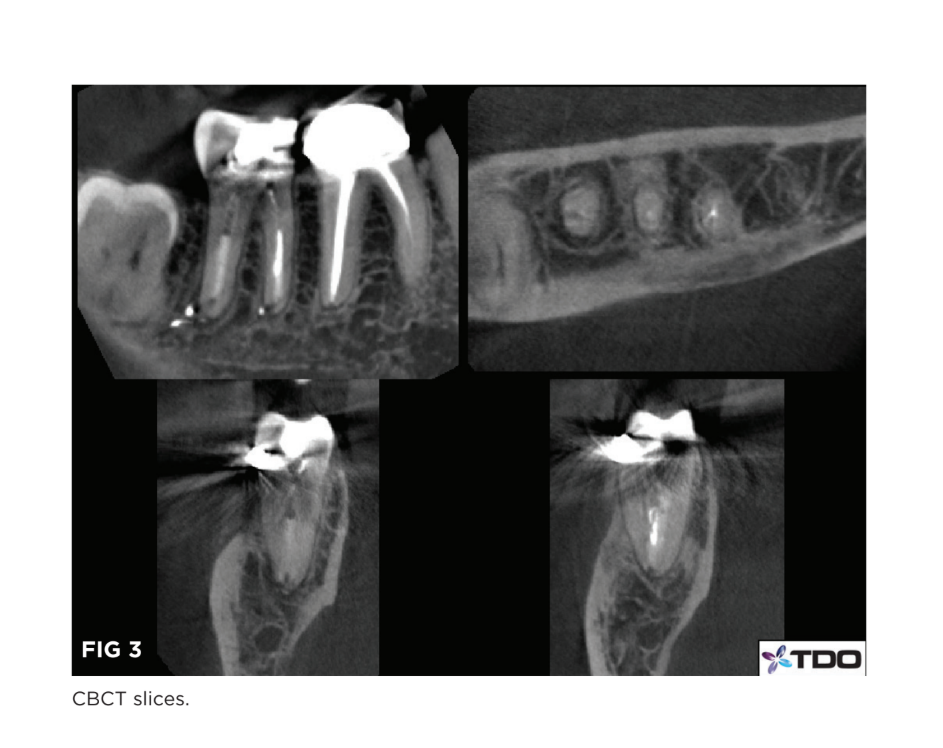
El paciente era un dentista masculino de 58 años con antecedentes de cáncer de tiroides. Se le había diagnosticado una enfermedad endodóntica recurrente en su segundo molar inferior derecho. El retratamiento fue iniciado por su endodoncista. Se presentó en mi consultorio quejándose de dolor a la percusión en el diente. Había visto a su endodoncista varias veces durante un período de varios meses sin mejora en sus síntomas. La oclusión era ligera en el diente. Las profundidades de sondaje periodontal eran normales y la transiluminación no mostró signos de fractura dental. Se realizó un diagnóstico de periodontitis apical sintomática. La tomografía CBCT (Fig. 3) no mostró evidencia de anatomía de conducto radicular no tratada ni fractura radicular.
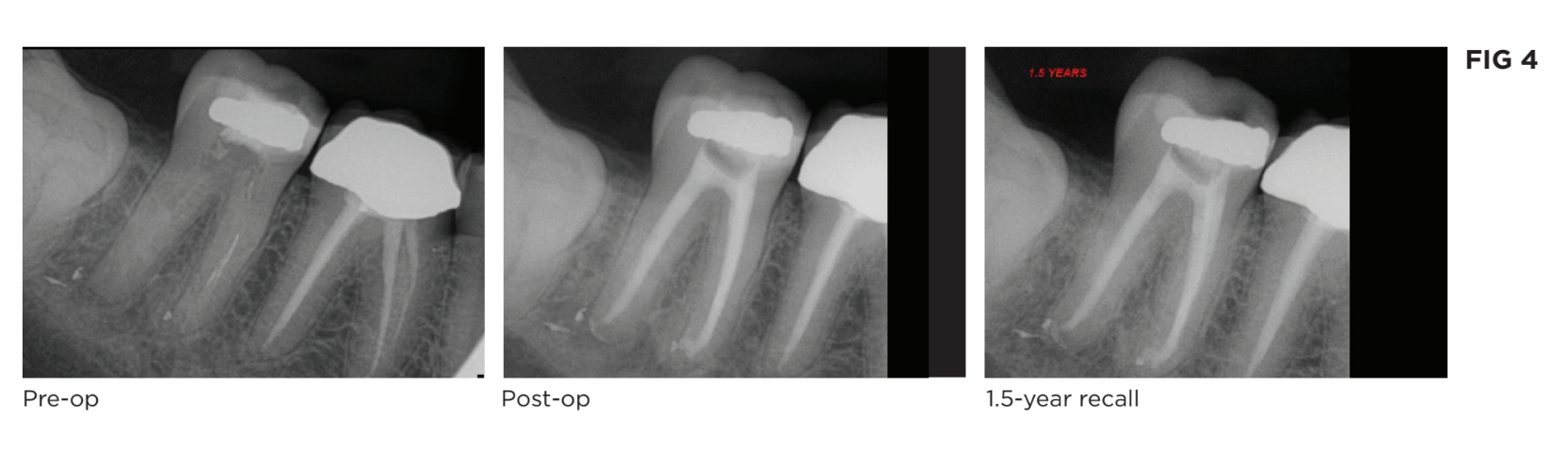
Bajo anestesia local, el diente (Fig. 4) fue tratado con el protocolo de Limpieza Apical Radial (RAC) y re-medicado con pasta de hidróxido de calcio. Se prescribió una receta de Amoxicilina 500mg TID durante siete días. En la segunda visita, tres semanas después, el diente estaba asintomático y fue obturado con un sellador biocerámico y la técnica de cono único de gutapercha (EndoSequence® BC Sealer and Points™, Brasseler, USA). En su seguimiento de un año y medio, el diente era funcional y asintomático con sondaje normal y evidencia radiográfica de curación completa. El diente aún no había sido restaurado permanentemente.
Informe de Caso #2
Una paciente femenina de 77 años se presentó con dolor e hinchazón asociada con su primer molar inferior izquierdo. Anteriormente había sido tratada por dos endodoncistas que no pudieron aliviar sus síntomas (Fig. 5).
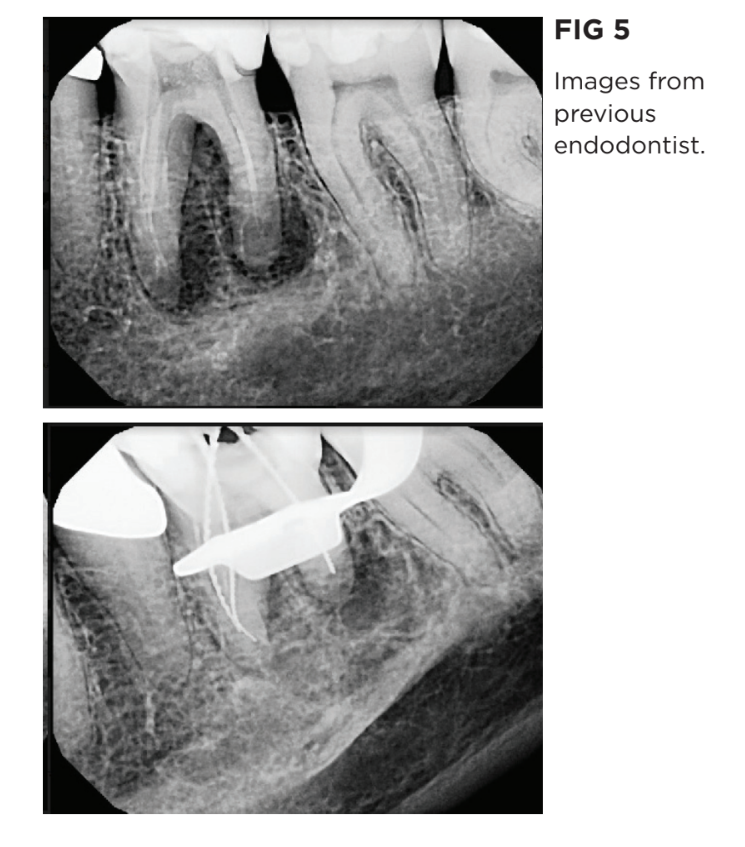
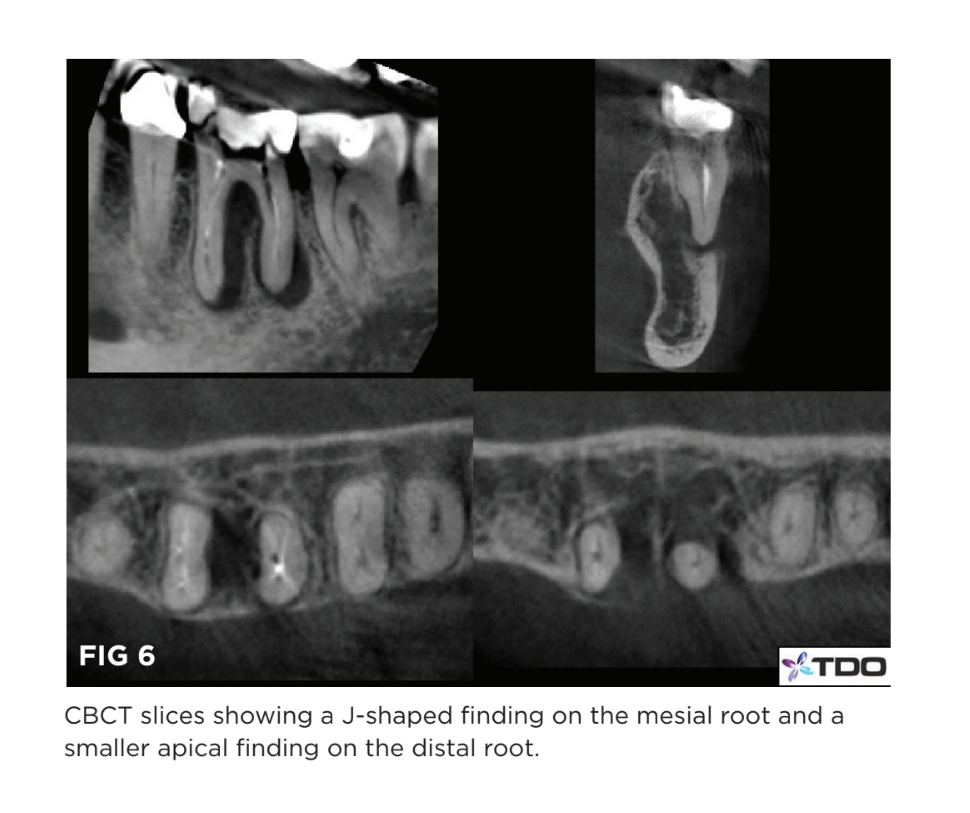
La examinación reveló hinchazón en el pliegue bucal adyacente y el diente era sensible a la percusión. La sondeo periodontal fue normal excepto por un estrecho bolsillo de 7 mm en el aspecto bucal de la raíz mesial. La transiluminación no mostró signos de un diente agrietado. El examen radiográfico mostró una radiolucidez en forma de J en la raíz mesial y una radiolucidez apical más pequeña en la raíz distal. La tomografía computarizada CBCT (Fig. 6) confirmó la extensión de los hallazgos así como evidencia de pérdida de la placa bucal en la raíz distal. Se realizó un diagnóstico de periodontitis apical sintomática con un seno de drenaje bucal a lo largo del espacio del ligamento periodontal.
Bajo anestesia local, el diente fue tratado con el protocolo de Limpieza Radial Apical (RAC) y re-medicado con pasta de hidróxido de calcio (Fig. 7). Se prescribió Amoxicilina 500 mg TID durante siete días. En la segunda visita, tres semanas después, el diente estaba asintomático y fue obturado con un sellador biocerámico y la técnica de gutapercha de cono único (Endo-Sequence® BC Sealer and Points™, Brasseler, USA).
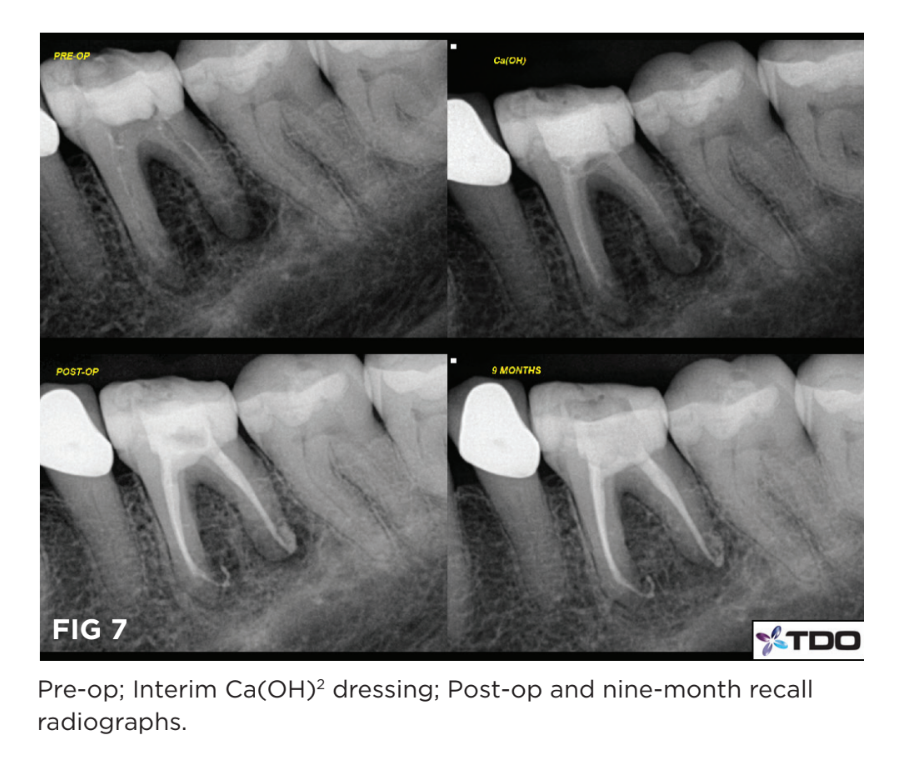
En el recall, nueve meses después, las profundidades de sondaje eran normales y el diente era funcional y asintomático con evidencia de curación ósea.
Limpieza Apical Radial (LAR)
La LAR es un protocolo de tratamiento que logra consistentemente una limpieza y desinfección superiores de sistemas de conductos radiculares complicados, utilizando un protocolo quimio-mecánico asistido por la aplicación de energía láser de disparo radial.
Elementos Principales del RAC
Instrumentación:
- Se establece un camino de deslizamiento con limas manuales .06 y .08 y limas rotativas de NiTi.
- Modelado apical profundo con limas de NiTi tratadas térmicamente, preservando siempre la estructura radicular, especialmente en el tercio coronal y la zona peri-cervical.
Irrigación:
- Irrigación efectiva con presión negativa apical utilizando el sistema EndoVacTM (Kavokerr) con solución de hipoclorito de sodio al 6%.
- Activación sónica del irrigante.
Limpieza:
Irrigación Activada por Láser (LAI) con láser Er,Cr:YSGG (Waterlase iPlus, Biolase, Irvine, CA) utilizando puntas láser RFT2 y RFT3 con configuraciones de 1.25 Watts, modo H, 20 Hz (PPS), 30% aire, 10% agua, 62.5 mJ/pulso.
Desinfección:
- Desinfección láser con láser Er,Cr:YSGG (Waterlase iPlus, Biolase, Irvine, CA) utilizando puntas láser RFT2 y RFT3 con configuraciones de 1.00 Watt, modo H, 20 Hz (PPS), 10% aire, 0% agua, 50 mJ/pulso.
- Desinfección profunda de la dentina con láser de diodo de 940 nm (Epic X, Biolase, Irvine, CA), con una punta láser no iniciada, utilizando configuraciones de 1 Watt, onda continua, en un canal húmedo. Este es un uso no aprobado del diodo en los EE. UU. ya que no se ha emitido ninguna autorización de la FDA para esta aplicación.
Idealmente, para la limpieza y desinfección, la punta del láser se coloca 1 mm por debajo de la longitud de trabajo y se activa al retirar la punta, en un movimiento circular, a una velocidad de 1-2 mm por segundo. Este proceso se repite cuatro veces en cada canal. La colocación de la punta del láser está influenciada por la anatomía del conducto radicular, el diámetro y la expansión del conducto preparado y la presencia o ausencia de permeabilidad del conducto; seguirá siendo efectiva incluso a distancias de 5 mm o más del foramen apical.
Lásers de Erbio en Endodoncia
Los láseres de erbio han surgido como la longitud de onda láser más prometedora en endodoncia. Son capaces tanto de tratar tejidos duros como blandos y tienen la mayor cantidad de aprobaciones de la FDA para una multitud de procedimientos dentales. Su cromóforo principal es el agua y en menor medida, el hidroxiapatito. Las interacciones foto-térmicas predominan en procedimientos de tejidos blandos y las interacciones foto-disruptivas en procedimientos de tejidos duros. Cuando se siguen los parámetros adecuados, la relajación térmica es excelente con un daño térmico colateral mínimo en los tejidos circundantes.
Acción en Sistemas de Conductos Radiculares
Cuando se activa en presencia de agua, ocurre una vaporización instantánea, creando una burbuja de vapor en el extremo de la punta del láser de disparo radial (Fig. 8). Las burbujas que se expanden rápidamente e implosionan crean un efecto de cavitación con chorros de agua de alta velocidad que forman tensión de corte a lo largo de la pared del conducto. Los efectos de cavitación secundarios de las irregularidades del conducto también contribuyen al potencial de limpieza y esterilización del tratamiento.

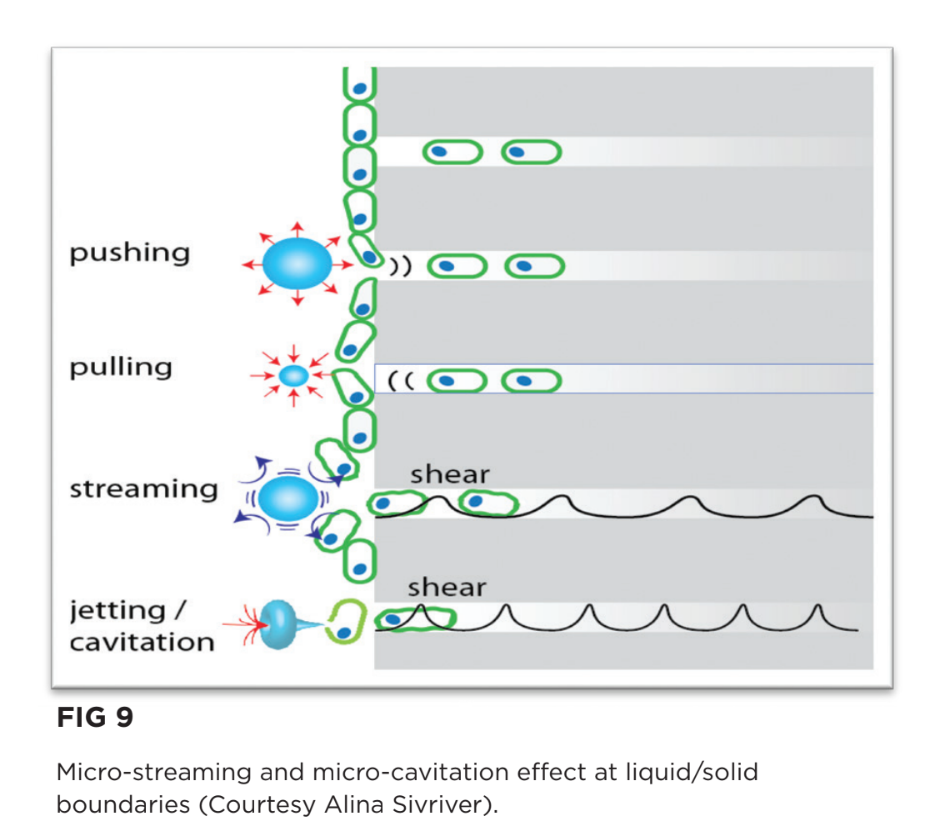
En los límites líquido-sólido (paredes del canal), se generan burbujas microscópicas por las fuerzas de cizallamiento de la onda acústica que pasa, lo que resulta en un efecto de micro-corriente y micro-cavitación que puede penetrar en las ramificaciones del canal y los túbulos dentinarios (Fig. 9). La expansión y colapso del agua intra-tubular es posible a una profundidad de 1,000 micrones o más, capaz de producir efectos acústicos lo suficientemente fuertes como para interrumpir el biofilm y matar bacterias.
Discusión
La enfermedad endodóntica es esencialmente una enfermedad mediada por biofilm y el éxito de la terapia endodóntica depende en gran medida de la capacidad para eliminar el biofilm y matar las bacterias del biofilm.
Para lograr este objetivo, la terapia endodóntica se ha basado en un desbridamiento quimio-mecánico del sistema de conductos radiculares. Debido a la complejidad de la anatomía del conducto radicular, aproximadamente el 30-45% del sistema de conductos radiculares permanece sin tocarse por la instrumentación mecánica y la sobreinstrumentación debilitará aún más el diente y puede influir en la iniciación de grietas apicales. Como resultado, se ha puesto más énfasis en la eficacia de los agentes desinfectantes para matar las bacterias del biofilm en lugar de las bacterias planctónicas. Las bacterias del biofilm pueden ser hasta 1,000 veces más resistentes a los agentes antibacterianos que sus contrapartes planctónicas.
Estudios anteriores han demostrado que la instrumentación y la irrigación antibacteriana con NaOCl eliminaron bacterias en el 50-75% de los conductos radiculares infectados al final de la primera sesión de tratamiento, mientras que los conductos radiculares restantes contenían bacterias recuperables. En su estudio, Nair et al. mostraron que el 88% de los molares mandibulares tratados en el conducto radicular mostraron infección residual de las raíces mesiales después de la instrumentación, irrigación con NaOCl y obturación en un tratamiento de una sola visita. Para que los agentes antimicrobianos sean efectivos, necesitan llegar al término del conducto, llevar partículas no disueltas, crear una corriente y reponerse continuamente. Chow ilustró que hay poco efecto de lavado más allá de la punta de una aguja de ventilación lateral. Además, la acción disolvente del hipoclorito de sodio sobre el tejido intracanal libera burbujas que pueden unirse para formar un bloqueo de vapor apical que promueve una mala limpieza apical al impedir que los irrigantes lleguen al término del conducto.
La irrigación por presión negativa apical ha demostrado ser extremadamente efectiva para superar estos obstáculos, pero se está volviendo cada vez más difícil de usar con las formas de canal más pequeñas que se abogan con los principios de endodoncia mínimamente invasiva.
La Irrigación Activada por Láser (LAI) genera ondas de estrés lo suficientemente fuertes como para interrumpir el biofilm, liberando así bacterias en su estado planctónico. Esto puede ocurrir ya sea debido a fallos cohesivos, interrumpiendo las capas superficiales, o fallos adhesivos, eliminando completamente el biofilm. Esto hace que las bacterias sean más susceptibles a los biocidas (irrigantes y medicamentos intracanal) utilizados para la desinfección del canal. También se ha informado de un efecto directo sobre las propias bacterias, aumentando la permeabilidad bacteriana al crear poros temporales en sus membranas y dañando las superficies celulares. Si las fuerzas de corte generadas son insuficientes para descomponer los enlaces cohesivos de la matriz del biofilm viscoelástico, el biofilm simplemente se deformará y volverá a su estado original. Pueden generarse fuerzas insuficientes con el uso de agitación sónica o ultrasónica o si la colocación de la punta del láser está demasiado distante del biofilm. También se ha demostrado que LAI elimina eficazmente la capa de arrastre y los tapones dentinarios, desempeñando así un papel importante en el mantenimiento y restablecimiento de la permeabilidad del canal. La eliminación del bloqueo de vapor apical es otra ventaja de LAI y ocurre mediante la interrupción de la tensión superficial en la interfaz solución-aire.
La desinfección con láser es un elemento importante de RAC y ocurre con la aplicación del láser Er,Cr:YSGG en modo seco. La energía del láser busca el agua en el tejido infectado, la matriz de biofilm altamente hidratada, así como las bacterias mismas, resultando en la ablación de los tejidos y microorganismos objetivo. El resultado final es una desinfección efectiva a una profundidad de 200 micrones en la dentina. Se ha informado de una desinfección de dentina más profunda con el láser de diodo y el enfoque de láser dual ha mostrado promesas in vitro. El cromóforo principal para la longitud de onda del láser de diodo es el pigmento (melanina y hemoglobina) y en menor medida, el agua. Esto resulta en una mayor penetración de luz a través de la dentina con poca interacción con ella, lo que hace posible buscar y destruir microorganismos más profundos en los túbulos dentinarios.
Conclusión
El desafío presentado por la enfermedad endodóntica refractaria puede resumirse en las palabras de Ricucci: “(Necesitamos) desarrollar estrategias, instrumentos o sustancias que puedan alcanzar esas áreas distantes del canal radicular principal para lograr una reducción suficiente en la carga biológica infecciosa que permita una curación perirradicular predecible”.
Se presenta un protocolo de tratamiento, Limpieza Radial Apical (RAC), para el manejo no quirúrgico de la enfermedad endodóntica refractaria. El protocolo se basa principalmente en un efecto sinérgico entre la irradiación láser Er,Cr:YSGG y la posterior irrigación con presión negativa apical con hipoclorito de sodio al 6%, que promueve la interrupción y destrucción de las bacterias del biofilm dentro de sistemas complejos de conductos radiculares y túbulos dentinarios. Si bien varios estudios se han centrado en identificar la microflora del conducto radicular en casos recalcitrantes en un intento de explicar la patogénesis de la enfermedad refractaria, esta autora sostiene que RAC es una herramienta valiosa capaz de tratar con éxito la carga biológica infecciosa, independientemente de la composición del biofilm en sí. En los dos informes de caso presentados, la única desviación significativa de los protocolos endodónticos estándar fue la introducción de la limpieza y desinfección endodóntica asistida por láser.
Referencias:
- Peters OA, Schönenberger K, Laib A. Efectos de cuatro técnicas de preparación de Ni-Ti en la geometría del conducto radicular evaluados por microtomografía computarizada. Int Endod J. 2001;34:221–30.
- Çapar İD, Uysal B, Ok E, Arslan H. Efecto del tamaño de la ampliación apical con instrumentos rotatorios, llenado de cono único, preparación del espacio para postes con taladros, extracción de postes de fibra y extracción de relleno de conducto radicular en la iniciación y propagación de grietas apicales. J Endod. 2015 Feb;41(2):253-6.
- Ceri H, Olson ME, Stremick C, Read RR, Morck D, Buret A. El dispositivo de biofilm de Calgary: nueva tecnología para la determinación rápida de las susceptibilidades a antibióticos de los biofilms bacterianos. J Clin Microbiol. 1999;37:1771–6.
- Byström A, Sundqvist G. Evaluación bacteriológica del efecto del hipoclorito de sodio al 0.5 por ciento en la terapia endodóntica. Oral Surg Oral Med Oral Pathol. 1983;55:307–12.
- Peters LB, van Winkelhoff AJ, Buijs JF, Wesselink PR. Efectos de la instrumentación, irrigación y vendaje con hidróxido de calcio en la infección en dientes sin pulpa con lesiones óseas periapicales. Int Endod J. 2002;35:13–21.
- Nair PN, Henry S, Cano V, Vera J. Estado microbiano del sistema de conducto radicular apical de molares mandibulares humanos con periodontitis apical primaria después de un "tratamiento endodóntico de una sola visita". Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2005;99:231–52.
- Chow TW. Efectividad mecánica de la irrigación del conducto radicular. J Endod. 1983 Nov;9(11):475-9.
- Nielsen BA, Baumgartner JC. Comparación del sistema EndoVac con la irrigación con aguja de conductos radiculares. J Endod 2007;33:611-5.
- Y. Krespi, et al. Disrupción láser de biofilm. Laryngoscope 2008;118:1168-1173.
- Gnanadhas, D. P. et al. Tratamiento exitoso de infecciones por biofilm utilizando ondas de choque combinadas con terapia antibiótica. Sci. Rep. 2015; 5,17440; doi: 10.1038/srep17440
- Arnabat J, Escribano C, Fenosa A, Vinuesa T, Gay-Escoda C, Berini L, Viñas M. Actividad bactericida del láser de erbio, cromo: itrio-escandio-galio-granate en conductos radiculares. Lasers Med Sci. 2010 Nov;25(6):805-10.
- Lopez-Jimenez L, Arnabat J, Vinas M, Vinuesa T. Visualización por microscopía de fuerza atómica de lesiones en la superficie de Enterococcus faecalis causadas por láseres Er,Cr:YSGG y de diodo. Med Oral Patol Oral Cir Bucal. 2014;Doi:10.4317/medoral.19991
- De Moor RJ, Blanken J, Meire M, Verdaasdonk R. Vapor explosivo inducido por láser y cavitación resultando en una irrigación efectiva del conducto radicular. Parte 2: evaluación de la eficacia. Lasers Surg Med. 2009 Sep;41(7):520-3.
- De Moor RJ, Meire M, Goharkhay K, Moritz A, Vanobbergen J. Eficacia de la irrigación activada por ultrasonido frente a la activada por láser para eliminar tapones de debris dentinarios colocados artificialmente. J Endod. 2010 Sep;36(9):1580-3.
- Peeters HH, De Moor RJ, Suharto D. Visualización de la eliminación de aire atrapado de la región apical en conductos radiculares simulados mediante irrigación activada por láser utilizando un láser Er,Cr:YSGG. Lasers Med Sci. 2015 Aug;30(6):1683-8.
- Peeters HH, Gutknecht N. Eficacia de la irrigación impulsada por láser frente a ultrasonido en la eliminación de un bloqueo de aire del tercio apical de un conducto radicular estrecho. Aust Endod J. 2014 Aug;40(2):47-53.
- Gordon W, Atabakhsh VA, Meza F, Doms A, Nissan R, Rizoiu I, Stevens RH. La eficacia antimicrobiana del láser de erbio, cromo: itrio-escandio-galio-granate con puntas de emisión radial en paredes de dentina de conducto radicular infectadas con Enterococcus faecalis. J Am Dent Assoc. 2007 Jul;138(7):992- 1002.
- Schoop U, Barylyak A, Goharkhay K, Beer F, Wernisch J, Georgopoulos A, Sperr W, Moritz A. El impacto de un láser de erbio, cromo: itrio-escandio-galio-granate con puntas de disparo radial en el tratamiento endodóntico. Lasers Med Sci 2009 Jan;24(1):59-65.
- Beer et al. Comparación de dos láseres de diodo en bactericidad en conductos radiculares: un estudio in vitro. Lasers in Med Sci. 2012;27;361-4.
- Hedge MN, Bhat R, Shetty P. Eficiencia de un láser de diodo semiconductor en la desinfección del sistema de conducto radicular en endodoncia: un estudio in vitro. J Int Clin Dent Res Organ 2015;7:35-8.
- Gutknecht N, Al-Karadaghi TS, Al-Maliky MA, Conrads G, Franzen R. El efecto bactericida de la irradiación láser de 2780 y 940 nm sobre Enterococcus faecalis en secciones de dentina bovina de diferentes grosores. Photomed Laser Surg. 2016 Nov;34(1);11-6.
- Al-Karadaghi TS, Gutknecht N, Jawad HA, Vanweersch L, Franzen R. Evaluación del aumento de temperatura durante el tratamiento de conductos radiculares con láser de doble longitud de onda: 2780 nm Er,Cr:YSGG y 940 nm de diodo. Photomed Laser Surg. 2015 Sep;33(9):460-6.
- Ricucci D, Loghin S, Siqueira JF Jr. Infección por biofilm exuberante en un canal lateral como causa de fracaso del tratamiento endodóntico a corto plazo: informe de un caso. J. Endod. 2013;39(5):712-8.
