Implantes de Disco Bioingenierizado para la Articulación Temporomandibular: Protocolo de Estudio para un Ensayo Piloto Preclínico Aleatorizado en Dos Fases en 18 Ovejas Merino Negras (TEMPOJIMS)
Traducción automática
El artículo original está escrito en idioma EN (enlace para leerlo) .
Resumen
Antecedentes: Los ensayos preclínicos son esenciales para probar opciones eficaces para sustituir el disco de la articulación temporomandibular (ATM). La ausencia contemporánea de un tratamiento ideal para pacientes con trastornos severos de la ATM puede estar relacionada con dificultades concernientes al diseño de estudio apropiado para llevar a cabo ensayos preclínicos en el campo de la ATM. Estas dificultades pueden estar asociadas con el uso de modelos animales heterogéneos, el uso de la ATM contralateral como control, la ausencia de ensayos preclínicos controlados aleatorios rigurosos con evaluadores de resultados cegados, y dificultades que involucran equipos multidisciplinarios.
Objetivo: Este estudio tiene como objetivo desarrollar un nuevo diseño de estudio reproducible y efectivo para la investigación preclínica en el dominio de la ATM, obteniendo datos rigurosos relacionados con (1) identificar el impacto de la discectomía bilateral en ovejas Merino negras, (2) identificar el impacto de la discopexia bilateral en ovejas Merino negras, y (3) identificar el impacto de tres discos de ATM de bioingeniería diferentes en ovejas Merino negras.
Métodos: Se propone un ensayo clínico preclínico aleatorizado exploratorio en dos fases con resultados ciegos. En la primera fase, nueve ovejas se aleatorizan en tres procedimientos quirúrgicos bilaterales diferentes: discectomía bilateral, discopéxia bilateral y cirugía simulada. En la segunda fase, nueve ovejas se aleatorizan para probar bilateralmente tres diferentes implantes de disco bioingeniería para la ATM. El resultado primario es la gradación histológica de la ATM. Los resultados secundarios son cambios en la imagen, tiempo masticatorio absoluto, tiempo de rumia por ciclo, cinética de rumia, área de rumia y peso de las ovejas.
Resultados: Los estudios preclínicos anteriores en este campo han utilizado el lado contralateral no operado como control, diferentes modelos animales que van desde ratones hasta un modelo canino, con diseños de estudio no aleatorizados, no ciegos y no controlados y medidas de resultados limitadas. El objetivo principal de este protocolo preclínico exploratorio es establecer un nuevo estándar para futuros ensayos preclínicos en cirugía oromaxilofacial, particularmente en el campo de la ATM, proponiendo un diseño riguroso en ovejas Merino negras. Los autores también pretenden probar la viabilidad de los resultados piloto. Los autores esperan aumentar la calidad de futuros estudios en este campo y avanzar en opciones de tratamiento para pacientes que se someten a cirugía de reemplazo de disco de la ATM.
Conclusiones: El estudio ha comenzado, pero es demasiado pronto para proporcionar resultados o conclusiones.
Introducción
La articulación temporomandibular (ATM) es la articulación más utilizada en el cuerpo humano. La ATM se abre y se cierra de 1500 a 2000 veces al día y es esencial para las funciones diarias de la boca, como la masticación, el habla, la deglución, el bostezo y el ronquido, involucrando una sinergia obligatoria especial de ambos lados articulares. El disco de la ATM es un componente esencial en la ATM normal y tiene las siguientes funciones: (1) distribuye la carga intraarticular, (2) estabiliza las articulaciones durante la traducción, y (3) disminuye el desgaste de la superficie articular. La mayoría de los trastornos de la ATM (TMD) se tratan con éxito con tratamientos reversibles, conservadores y de baja tecnología, como la educación y el asesoramiento, ejercicios terapéuticos, terapia de férulas y farmacoterapia.
Cuando el disco de la ATM está desplazado, malformado o dañado, puede inducir seriosos procesos patológicos internos y/o osteoartritis. Actualmente, los pacientes que sufren de TMD severo tienen opciones de tratamiento validadas limitadas. La mayoría de los enfoques quirúrgicos, como la discectomía de la ATM, no restauran las propiedades estructurales o biológicas de la articulación y el disco. Este procedimiento puede no ser ideal porque la ATM queda sin una estructura funcional importante. Se han utilizado una variedad de materiales interposicionales para reemplazar los discos removidos, incluidos materiales sintéticos fabricados a partir de silicona, Teflón, politetrafluoroetileno y injertos interposicionales biológicos tomados de diferentes sitios anatómicos. Estos materiales interposicionales no tienen en cuenta la anatomía y las características bioquímicas y biomecánicas del disco nativo de la ATM, y algunos de ellos se han asociado con complicaciones graves para los pacientes. A finales de la década de 1980, se descubrió que los implantes Proplast/Teflón de la ATM (implante interposicional sintético) eran perjudiciales en muchos pacientes. La descomposición del material, probablemente causada por las altas fuerzas biomecánicas de la ATM, llevó a partículas fragmentadas que resultaron en una respuesta inmune de cuerpo extraño que causó problemas que iban desde reacciones inflamatorias cutáneas severas en las áreas preauricular y de mejilla hasta enfermedades articulares degenerativas severas con perforación en la fosa craneal media. El resultado fue un espectro clínico dramático de fallas para estos implantes. En diciembre de 1991, el boletín de la Administración de Alimentos y Medicamentos de EE. UU. recomendó la eliminación inmediata de todos los implantes Proplast/Teflón de la ATM anteriores debido a las fallas mecánicas, muchas de las cuales resultaron en degeneración ósea progresiva. En un taller de 1992, la Academia Americana de Cirugía Oral y Maxilofacial instruyó la discontinuación de Proplast/Teflón.
La ausencia de opciones eficaces para sustituir el disco de la ATM puede estar relacionada con las dificultades en la traducción de la evidencia animal a la práctica clínica en humanos. Estas limitaciones probablemente están relacionadas con:
el uso de modelos animales heterogéneos con resultados contradictorios, posiblemente debido a la anatomía variable y la carga intraarticular entre especies;
el uso de la ATM contralateral como control, que puede estar asociado con la sobrecarga contralateral;
los biomateriales utilizados para reemplazar el disco no tienen en cuenta las características morfológicas y biomecánicas del disco nativo;
la ausencia de ensayos controlados aleatorios con cegamiento de los evaluadores de resultados; y
la falta de equipos multidisciplinarios involucrados en el proyecto.
La investigación preclínica debe promover la traducción efectiva del conocimiento a la práctica. Los aspectos mencionados anteriormente pueden limitar la traducción efectiva del conocimiento científico de calidad a la práctica clínica y pueden presentar problemas potenciales para los pacientes, clínicos y el progreso científico.
La ausencia contemporánea de opciones exitosas para sustituir el disco de la ATM sigue siendo un problema importante para la salud pública. Poco ha cambiado en la última década en cuanto a los diseños de estudio para la investigación de la ATM, y el tratamiento para pacientes con TMD severo sigue siendo controvertido. El objetivo principal del Estudio de Material de Interposición de la Articulación Temporomandibular (TEMPOJIMS) es desarrollar un nuevo diseño de estudio reproducible y efectivo para la investigación preclínica en el campo de la ATM. El segundo objetivo es avanzar en bioingeniería y medicina regenerativa evaluando los beneficios de un implante de bioingeniería de la ATM para sustituir el disco nativo dañado de la ATM. Este estudio exploratorio preclínico se divide en dos fases. La Fase 1 de este estudio es un ensayo preclínico aleatorizado y ciego, diseñado para investigar si la ATM sufre una lesión importante en la discectomía bilateral, discopexia bilateral y cirugía simulada. Las intenciones de la Fase 2 son evaluar la seguridad y eficacia de tres diferentes implantes de bioingeniería de la ATM utilizando el mismo método riguroso de la fase 1.
Métodos
Diseño del Estudio
El TEMPOJIMS es un ensayo clínico preclínico controlado aleatorio exploratorio de dos fases planeado para recopilar información preliminar para (1) evaluar un nuevo diseño de estudio para la investigación del ATM; (2) evaluar el modelo animal de oveja Merino negra para la investigación del ATM; (3) evaluar el comportamiento del ATM bajo intervención quirúrgica bilateral (discectomía y discopexia) utilizando un resultado primario histológico (puntuación microscópica de cambios destructivos en el ATM utilizando un sistema de puntuación Mankin modificado), resultado secundario de imagen (puntuación de imagen del ATM); (4) probar la aplicabilidad de resultados secundarios piloto predominantemente para la cinética de rumiantes; y (5) obtener una línea base para la interpretación de los resultados de implantes bioingenieriles de disco del ATM. La Fase II tiene como objetivo probar la seguridad y eficacia de tres diferentes implantes de disco bioingenieril bilateral del ATM (Figura 1). Los evaluadores y analistas de resultados están cegados para las evaluaciones quirúrgicas.
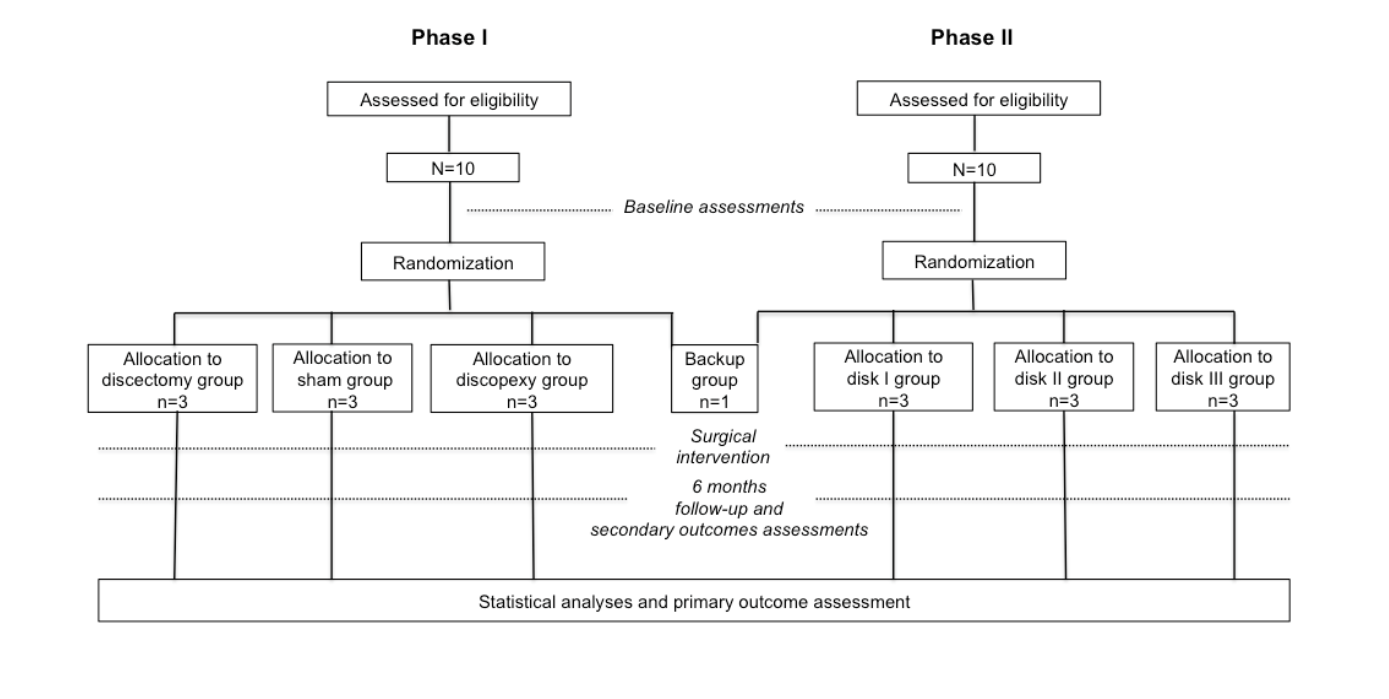
Las principales instituciones involucradas en este estudio son (1) la Facultad de Medicina de Lisboa para el diseño del estudio, coordinación y análisis estadístico; (2) el Centro Interdisciplinario de Investigación en Salud Animal de la Facultad de Medicina Veterinaria para la preparación histológica y el apoyo veterinario de todos los animales; (3) el Centro para el Desarrollo Rápido y Sostenible de Productos para implantes de discos bioingenierizados (discos I y II); (4) Bioingeniería, Cirugía, Ingeniería Química, Ingeniería Mecánica y Ciencia de Materiales, Universidad de Pittsburgh, para implantes de discos bioingenierizados (disco III); (5) el Departamento de Cirugía Oral y Maxilofacial-Cabeza y Cuello, Hospital Universitario Infanta Cristina, Badajoz, España, para apoyo quirúrgico; (6) el Instituto de Investigación de Huesos y Articulaciones-Distrito de Salud Local del Norte de Sídney-Escuela de Medicina de Sídney del Norte, Universidad de Sídney, Australia, para análisis histológico; y (7) el Departamento de Radiología del Hospital Santa María, Lisboa, Portugal, para análisis de imágenes.
Modelo Animal
Se han utilizado diversas cepas/razas de ovejas en investigaciones sobre la ATM. Para disminuir la variabilidad biológica, los autores recomendaron las ovejas Merino negras como el modelo animal para llevar a cabo el estudio. Como se recomendó, los autores propusieron utilizar “ovejas esqueléticamente maduras” de ≥2 años de edad. Los criterios de inclusión son ovejas Merino negras certificadas, adultas (edad de 2 a 5 años), hembras y en buen estado de salud (se realiza un chequeo veterinario a todos los animales). En cuanto a las consideraciones éticas sobre los animales, el diseño del estudio fue aprobado por la Autoridad Nacional Portuguesa de Salud Animal registrada con el número 026618. El diseño y la organización del estudio respetan las pautas de Investigación Animal: Informe de Experimentos In Vivo (ARRIVE).
Evaluación Basal y de Seguimiento
Las evaluaciones basal y de seguimiento se describen en momentos específicos (Figura 2). Los resultados secundarios piloto y el peso se miden en los días 11, 10 y 9 antes de la cirugía (los detalles sobre los resultados secundarios se informan en las medidas de resultados). El transporte a las instalaciones quirúrgicas se realiza 5 días antes de la cirugía para evitar el estrés animal y permitir la familiarización con las instalaciones temporales. Se realiza una tomografía computarizada (TC) de cabeza el día de la cirugía aprovechando la sedación preanestésica. Diez días después de la cirugía, los animales son transportados a las instalaciones principales de TEMPOJIMS. Los días 19, 20 y 21 después de la cirugía, se comienzan a registrar los resultados secundarios de seguimiento cada 30 días durante 6 meses (Figura 2). Al final, los animales son sacrificados y se realiza una nueva TC para medir el resultado de imagen y comenzar la preparación histológica.
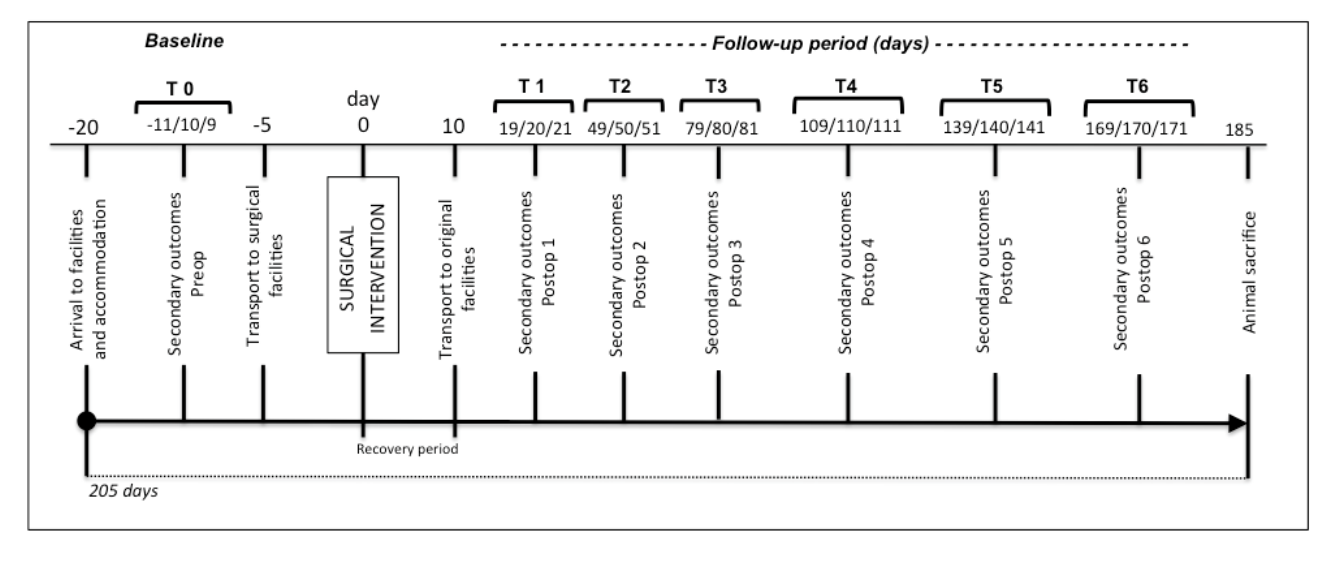
Randomización, Asignación y Cegamiento
La aleatorización es realizada por un grupo estadístico no involucrado en las evaluaciones de resultados, gestionado por la Facultad de Medicina de Lisboa. La asignación a cada grupo aleatorizado se realiza de manera preoperatoria mediante un sobre sellado y por separado para la fase 1 y la fase 2 del estudio. El equipo quirúrgico no está cegado a la asignación del tratamiento dado el tipo de intervención; sin embargo, los miembros del equipo quirúrgico no están involucrados en las evaluaciones de resultados. Todos los evaluadores de resultados están cegados a la intervención. En la fase 1, se asignan 10 ovejas al grupo de intervención: grupo de cirugía simulada (n=3), grupo de discectomía (n=3), grupo de discopexia (n=3) y grupo de respaldo (n=1). Se planea utilizar la oveja de respaldo si ocurre la muerte debido a la anestesia o a otra complicación no relacionada con la intervención quirúrgica. En la fase 2, se asignan aleatoriamente 10 ovejas al grupo disco I (n=3), grupo disco II (n=3), grupo disco III (n=3) y grupo de respaldo (n=1) (Figura 1).
Fase de Intervención
Protocolo de Anestesia
Se requiere ayuno y restricción de agua 24 horas antes de la cirugía. La sedación se realiza con diazepam (0.5 mg/kg iv), seguida de la inducción de anestesia con ketamina (5 mg/kg iv). Se realiza intubación oral y la anestesia se mantiene con isoflurano (1.5% a 2%). Para asegurar la analgesia del animal, se administra meloxicam (0.5 mg/kg iv, bid) el día de la cirugía y durante 4 días postoperatorios. Se utiliza profilaxis antibiótica con amoxicilina y ácido clavulánico durante 5 días.
Protocolo de Intervención Quirúrgica para las Fases 1 y 2
Fase 1
Discectomía bilateral (n=3): bajo anestesia general, el equipo quirúrgico realiza una incisión en la piel preauricular y una disección roma del tejido blando que cubre la articulación. Se expone el área de la articulación y se incide la cápsula articular. Se identifican el disco y sus anexos. Se desprenden los anexos medial, anterior, posterior y lateral del disco y se realiza la discectomía. La herida se cierra en capas.
Discopexia bilateral (n=3): bajo anestesia general, el equipo quirúrgico realiza una incisión en la piel preauricular y una disección roma del tejido blando que cubre la articulación. Se expone el área de la articulación y se incide la cápsula articular. Se identifican el disco y sus fijaciones. Las fijaciones laterales y posteriores del disco se desprenden y se suturan con poli- p-dioxanona (PDS) 3/0. La herida se cierra en capas.
Cirugía simulada (n=3): bajo anestesia general, el equipo quirúrgico realizará una incisión en la piel preauricular y una disección roma del tejido blando que cubre la articulación. La cápsula no se incide. La herida se cierra en capas.
Fase 2
Disco I (n=3): bajo anestesia general, el equipo quirúrgico realiza una incisión en la piel preauricular y una disección roma del tejido blando que cubre la articulación. Se expone el área de la articulación y se incide la cápsula articular. Se identifican el disco y sus fijaciones. Las fijaciones medial, anterior, posterior y lateral del disco se desprenden y se realiza una discectomía. El disco I se introduce en el espacio articular y se sutura en las fijaciones laterales. La herida se cierra en capas. El disco I será un biomaterial alternativo y por razones intelectuales no puede ser revelado en este documento.
Disco II (n=3): bajo anestesia general, el equipo quirúrgico realiza una incisión en la piel preauricular y una disección roma del tejido blando que cubre la articulación. Se expone el área de la articulación y se incide la cápsula articular. Se identifican el disco y sus uniones. Se desprenden las uniones medial, anterior, posterior y lateral del disco y se realiza una discectomía. El disco II se introduce en el espacio articular y se sutura en las uniones laterales. La herida se cierra en capas. El disco II será un andamiaje poroso de poli(glicerol sebacato) (PGS) reforzado con policaprolactona (PCL).
Disco III (n=3): bajo anestesia general, el equipo quirúrgico realiza una incisión en la piel preauricular y una disección roma del tejido blando que cubre la articulación. Se expone el área de la articulación y se incide la cápsula articular. Se identifican el disco y sus uniones. Se desprenden las uniones medial, anterior, posterior y lateral del disco y se realiza una discectomía. El disco III se introduce en el espacio articular y se sutura en la unión lateral. La herida se cierra en capas. El disco III será un andamiaje poroso de PGS preparado mediante un método modificado de fusión de sal. Brevemente, partículas de sal molidas (150 mg) con un tamaño de entre 25 y 32 µm se colocarán en un molde impreso en 3D. El molde se transferirá a un incubador a 37°C y 90% de humedad relativa durante 1 hora. Las plantillas fusionadas de partículas de sal se secarán en un horno de vacío a 90°C y 100 millitorr (mTorr) durante la noche, retirando cuidadosamente el pastel de sal del molde antes de un procesamiento adicional. PGS recién hecho disuelto en tetrahydrofuran (THF; 20 wt%, 380 µL, sal:PGS=2:1) se añade al pastel de sal, y se permite que el THF se evapore completamente en una campana de extracción durante 30 minutos. El pastel de sal se transfiere a un horno de vacío y se cura a 150°C y 100 mTorr durante 24 horas. Las plantillas de sal impregnadas de PGS resultantes se sumergen en agua desionizada durante 4 horas, y luego se reemplazan con agua durante 4 horas, con intercambio de agua cada 4 horas durante las primeras 12 horas. Después del baño de agua de 12 horas, los andamiajes se transfieren a agua desionizada durante otras 24 horas con intercambio de agua cada 8 horas. Los andamiajes resultantes se congelan a -80°C y luego se aplica el proceso de liofilización.
Se contemplan diez días para la recuperación en el cuidado de heridas y medicación postoperatoria (ver Figura 2).
Medidas de Resultado
El resultado primario es la puntuación microscópica de los cambios destructivos en la ATM utilizando un sistema de puntuación Mankin modificado. Los resultados secundarios son la puntuación por imágenes de los cambios destructivos en la ATM, el tiempo masticatorio absoluto, el tiempo de rumia por ciclo, la cinética de rumia, el área de rumia y el peso corporal de las ovejas. Los parámetros de resultado primarios y secundarios se describen con más detalle en Figura 3.
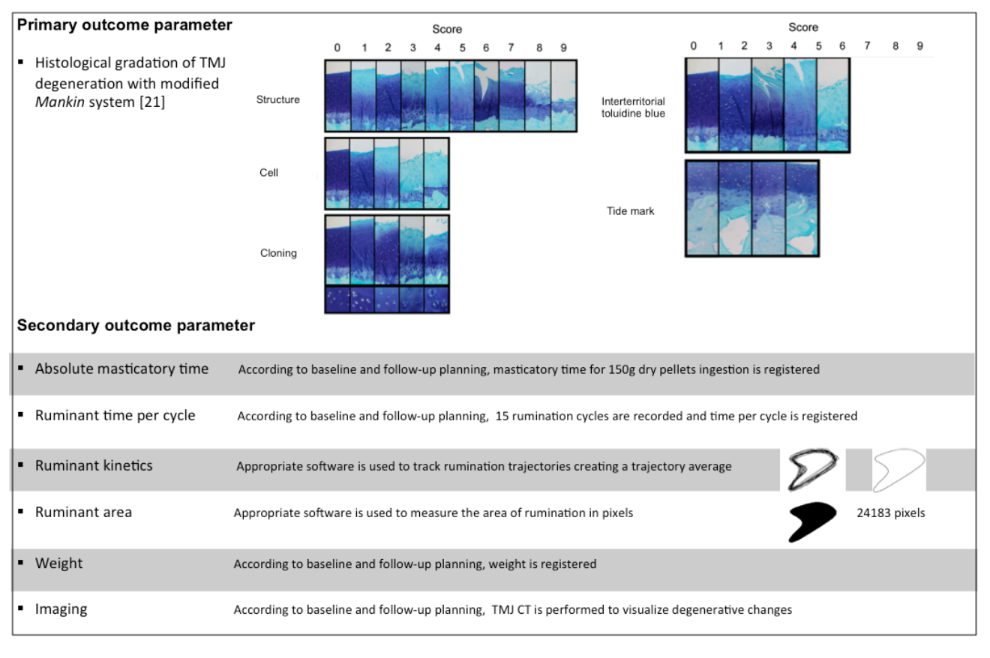
Resultado Primario
El objetivo es evaluar la gradación histológica de los cambios destructivos de la ATM. El punto de tiempo es 6 meses después de la intervención quirúrgica.
Seis meses después de la cirugía, se retira la ATM utilizando una sierra oscilante de hueso de necropsia de acuerdo con las siguientes referencias anatómicas: craneal (aspecto craneal del proceso coronoides en la región de unión del proceso cigomático), caudal (externo al meato acústico), dorsal (la referencia se establece en el hueso temporal escamoso) y ventral (la referencia se fija 2 cm por debajo del meato acústico en la zona del ángulo estilohioideo). Las articulaciones se fijan en formalina tamponada al 10% durante 24 horas y se almacenan en etanol al 70%. La descalcificación se obtiene mediante inmersión en ácido fórmico al 10% en formalina al 5% durante hasta 20 días, después de lo cual las articulaciones se cortan sagitalmente a través de todo el cóndilo. Después de la descalcificación, las articulaciones de la ATM se sumergen en tres mezclas graduadas de salicilato de metilo/parafina y se cortan sagitalmente desde la parte lateral hasta la parte central de la ATM. Las secciones histológicas se envían al Instituto de Investigación de Huesos y Articulaciones de Sídney para la puntuación histológica utilizando un sistema de puntuación Mankin modificado. Esta evaluación se realiza y clasifica de manera independiente por dos histologistas que estarán cegados a la intervención. Un tercer histologista actuará como árbitro en caso de disparidad.
Resultados Secundarios
Las características evaluadas son análisis de imágenes, tiempo absoluto de masticación, tiempo de rumia por ciclo, cinemática de rumia, área de rumia y peso de las ovejas (ver Apéndices Multimedia 1 y 2). El punto de tiempo es cada mes después de la intervención quirúrgica durante un total de 6 meses.
Para medir los resultados secundarios, se construyó una jaula específica (ver Figura 4) con una ventana frontal y un comedero.
Análisis de imágenes: se realiza una TC preoperatoria en todas las ovejas. Después del sacrificio del animal, se escanean los bloques de la ATM por TC y se realiza la evaluación de imágenes utilizando los criterios y la puntuación descritos en Tabla 1.
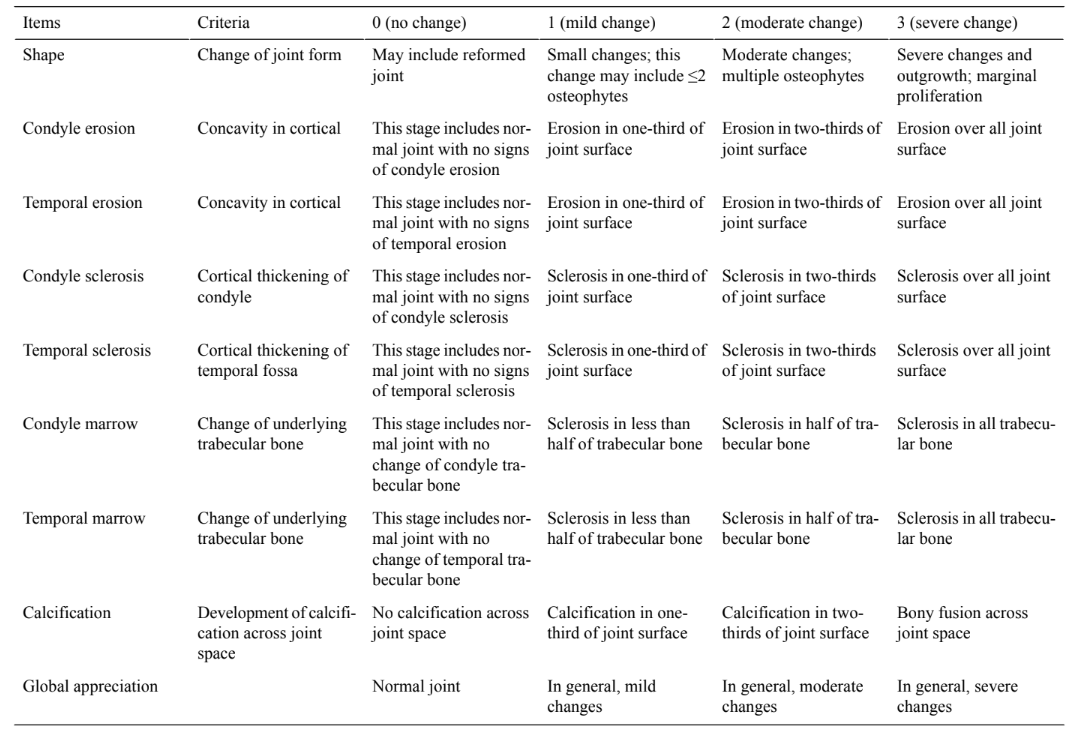

Esta evaluación es realizada y clasificada de manera independiente por dos radiólogos experimentados que estarán cegados a la intervención. Un tercer radiólogo actuará como árbitro en caso de disparidad.
Tiempo masticatorio absoluto: respetando el diagrama de flujo (Figura 2), a las 9:00 am los animales son colocados en jaulas individuales. Se introduce una dosis de 150 gramos de pellets secos (Rico Gado A3) en el comedero y se mide el tiempo hasta que comen todos los pellets con un cronómetro (ver Apéndice Multimedia 1).
Tiempo de rumia por ciclo: respetando el cronograma (Figura 2), registramos 15 ciclos de rumia aproximadamente 4 horas después de la alimentación de 150 gramos. Usamos una cámara de video Canon 7D y grabamos imágenes a 25 fotogramas por segundo. Luego, el número de fotogramas por ciclo se divide por 25 para obtener el tiempo en segundos por ciclo (ver Apéndice Multimedia 2).
Cinetica de rumiantes: utilizamos el software Foundry Nuke (seguimiento 2D) para realizar el seguimiento rumiatorio y obtener el promedio del ciclo rumiatorio. Con el software After Effects , convertimos el seguimiento 2-D en una forma geométrica (ver Apéndice Multimedia 2).
Área de rumiantes: determinamos el promedio de 15 ciclos y creamos una forma geométrica. Usando el software Image J, realizamos una medida cuantitativa en píxeles del promedio del área rumiantes.
Peso: de acuerdo con el horario, después de comer 150 gramos de pellets secos, se pesa a las ovejas (ver Apéndice Multimedia 1).
Todas las evaluaciones son realizadas por investigadores que están cegados a la intervención quirúrgica.
Análisis Estadísticos
Todos los análisis estadísticos se realizarán utilizando la versión 22 de SPSS (IBM Corp, Armonk, NY, EE. UU.). Se realizará un análisis transversal para comparar las variables de resultado en los tres niveles de la variable independiente antes y después de la asignación del grupo de tratamiento aleatorizado. En los análisis transversales, se realizará un análisis de varianza de una vía (ANOVA), después de probar todas las suposiciones. Para el análisis longitudinal, se realizará un ANOVA de una vía con medidas repetidas tomando como efectos dentro de los sujetos las observaciones después de la cirugía (meses 1 a 6). Se realizarán pruebas post hoc de la diferencia mínima significativa de Fisher para verificar diferencias significativas para los diferentes tratamientos.
Informe de Eventos Adversos
Se considerarán eventos adversos relacionados con el estudio, incluyendo (1) eventos de anestesia: muerte idiopática, neumotórax, otras complicaciones relacionadas con la anestesia; (2) técnica quirúrgica: sangrado masivo, fractura condilar, otras complicaciones relacionadas con la técnica quirúrgica; y (3) eventos postoperatorios: infección de la ATM, dehiscencia de sutura, disminución del apetito, paresia facial, disminución de la rumia, disminución de peso.
Discusión
Este estudio investiga los efectos y efectos adversos de (1) discectomía bilateral, (2) discopexia bilateral y (3) implantes de disco bioingenierizados. Aunque este estudio preclínico servirá principalmente como un estudio piloto, esperamos obtener una mejor comprensión de los cambios morfológicos e histológicos en la ATM y las implicaciones en la cinética masticatoria.
Hasta ahora, los resultados sobre la discectomía son contradictorios. Estudios preclínicos anteriores en este campo han utilizado el lado contralateral no operado como control y diferentes modelos animales que van desde ratones hasta un modelo canino. Usar el lado contralateral como control puede ser inapropiado considerando la influencia de la sobrecarga contralateral. Teóricamente, esperamos reducir este sesgo utilizando un enfoque bilateral. La variabilidad animal en los diferentes estudios es una advertencia sobre la importancia de usar el mismo modelo animal en futuros estudios sobre investigaciones de implantes de ATM. Por lo tanto, nuestro grupo realizó un estudio previo considerando ovejas Merino negras como un modelo animal prometedor para estudios sobre la investigación de implantes de disco de ATM, prótesis de ATM y modelo de osteoartritis de ATM. Para aumentar la calidad de TEMPOJIMS, los autores utilizarán un grupo de control de cirugía simulada.
Esperamos obtener información valiosa relacionada con el grupo de discopexia de fase 1 respecto a si el enfoque quirúrgico promueve daño intraarticular. Esto puede mejorar las conclusiones futuras sobre la atribución de posibles daños a la intervención en sí en lugar del implante de ATM. Esta pregunta es importante considerando que se requerirá un enfoque quirúrgico para colocar implantes de ATM en la fase 2. Nuevamente, utilizar una intervención bilateral podría reducir un posible sesgo.
La mayoría de los estudios preclínicos se han centrado en evaluaciones morfológicas/histológicas generales y no fueron diseñados para caracterizar el movimiento articular alterado fundamental (cinética) o las consecuencias funcionales. En este estudio, incluimos resultados secundarios piloto para evaluar cambios en la cinética de rumiantes. Esperamos correlacionar los resultados primarios con los secundarios para entender si pueden ser utilizados en futuros estudios de ATM. Puede ser interesante entender varios elementos:
- ¿Existen diferencias en el tiempo masticatorio entre los grupos de disco versus discectomía y discopéxia?
- ¿Hay una correlación entre los resultados histológicos, de imagen y cinéticos?
- ¿Cambia el área y la geometría rumiantes al realizar diferentes intervenciones?
- ¿Hay una diferencia en la cinética rumiantes entre los grupos de disco versus discectomía y discopéxia?
- ¿Los implantes de ATM aceleran la osteoartritis?
En cuanto a la fase 2, la elección del biomaterial es crítica. El implante de ATM estará expuesto a un entorno mecánico y estresante con un suministro limitado de sangre que puede limitar la migración celular y la regeneración in situ. Probar tres discos de bioingeniería diferentes in vivo y correlacionar in vitro con el comportamiento in vivo puede mejorar seriamente las estrategias de bioingeniería para lograr un implante de disco de ATM seguro y eficaz para humanos.
La principal fortaleza de este estudio es el modelo animal propuesto; los resultados convencionales y piloto descritos; el diseño del estudio con un grupo de control aleatorizado, ciego y placebo; y el uso de procedimientos quirúrgicos bilaterales. Las limitaciones potenciales del estudio incluyen el tamaño de muestra relativamente pequeño. Si este estudio confirma la viabilidad del protocolo propuesto y la eficacia inicial de los implantes de disco de la ATM planificados, se justificaría un ensayo preclínico más grande para determinar aún más la efectividad de estos discos y promover la traducción de la evidencia animal a la práctica clínica en humanos.
Autores: David Faustino Ângelo, Florencio Gil Monje, Raúl González-García, Christopher B Little, Lisete Mónico, Mário Pinho, Fábio Abade Santos, Belmira Carrapiço, Sandra Cavaco Gonçalves, Pedro Morouço, Nuno Alves, Carla Moura, Yadong Wang, Eric Jeffries, Jin Gao, Rita Sousa, Lia Lucas Neto, Daniel Caldeira, Francisco Salvado
Referencias
- Bae Y, Park Y. El efecto de los ejercicios de relajación para los músculos masticadores en la disfunción de la articulación temporomandibular (ATM). J Phys Ther Sci 2013;25(5):583-586. [doi: 10.1589/jpts.25.583]
- Allen K, Athanasiou K. Ingeniería de tejidos del disco de la ATM: una revisión. Tissue Eng 2006;12(5):1183-1196. [doi: 10.1089/ten.2006.12.1183]
- Tanaka E, Sasaki A, Tahmina K, Yamaguchi K, Mori Y, Tanne K. Propiedades mecánicas del disco articular humano y su influencia en la carga de la ATM estudiada con el método de elementos finitos. J Oral Rehabil 2001 Mar;28(3):273-279. [Medline: 11394374]
- Martins-Júnior RL, Palma Antônio JC, Marquardt EJ, Gondin TM, Kerber FD. Trastornos temporomandibulares: un informe de 124 pacientes. J Contemp Dent Pract 2010 Oct 14;11(5):71-78. [Medline: 20978727]
- Navrátil L, Navratil V, Hajkova S, Hlinakova P, Dostalova T, Vranová J. Tratamiento integral de los trastornos de la articulación temporomandibular. Cranio 2014 Jan;32(1):24-30. [doi: 10.1179/0886963413Z.0000000002] [Medline: 24660643]
- Mehra P, Wolford LM. El ancla mini Mitek para el reposicionamiento del disco de la ATM: técnica quirúrgica y resultados. Int J Oral Maxillofac Surg 2001 Dec;30(6):497-503. [doi: 10.1054/ijom.2001.0163] [Medline: 11829231]
- Al-Baghdadi M, Durham J, Araujo-Soares V, Robalino S, Errington L, Steele J. Manejo del desplazamiento del disco de la ATM sin reducción: una revisión sistemática. J Dent Res 2014 Jul;93(7 Suppl):37S-51S [Texto completo GRATIS] [doi: 10.1177/0022034514528333] [Medline: 24659775]
- Estabrooks L, Fairbanks C, Collett R, Miller L. Una evaluación retrospectiva de 301 implantes Proplast-Teflon de la ATM. Oral Surg Oral Med Oral Pathol 1990 Sep;70(3):381-386. [Medline: 2216373]
- Henry CH, Wolford LM. Resultados del tratamiento para la reconstrucción de la articulación temporomandibular después del fallo del implante Proplast-Teflon. J Oral Maxillofac Surg 1993 Apr;51(4):352-358; discusión 359. [Medline: 8450350]
- Mercuri LG, Giobbie-Hurder A. Resultados a largo plazo después de la reconstrucción total de la articulación temporomandibular aloplástica tras la exposición a materiales fallidos. J Oral Maxillofac Surg 2004 Sep;62(9):1088-1096. [Medline: 15346359]
- Morouço P, Ângelo D, Francisco L, Moura C, Alves N. Ingeniería de tejidos para la reparación y regeneración del disco de la articulación temporomandibular: una perspectiva metodológica. Adv Cell Mol Otolaryngol 2017 Jan 17;4(1):33709. [doi: 10.3402/acmo.v4.33709]
- Lypka M, Yamashita DR. Reacción exuberante de células gigantes de cuerpo extraño a un implante de teflón/proplast de la articulación temporomandibular: informe de un caso. J Oral Maxillofac Surg 2007 Sep;65(9):1680-1684. [doi: 10.1016/j.joms.2006.09.030] [Medline: 17719383]
- Spagnoli D, Kent JN. Evaluación multicéntrica del implante de disco Proplast-Teflon de la articulación temporomandibular. Oral Surg Oral Med Oral Pathol 1992 Oct;74(4):411-421. [Medline: 1408011]
- Fricton JR, Look JO, Schiffman E, Swift J. Estudio a largo plazo de la cirugía de la articulación temporomandibular con implantes aloplásticos en comparación con cirugía sin implantes y rehabilitación no quirúrgica para el desplazamiento doloroso del disco de la articulación temporomandibular. J Oral Maxillofac Surg 2002 Dec;60(12):1400-1411; discusión 1411. [doi: 10.1053/joms.2002.36091] [Medline: 12465000]
- Kulber DA, Davos I, Aronowitz JA. Reacción cutánea severa de células gigantes de cuerpo extraño después de la reconstrucción de la articulación temporomandibular con Proplast-Teflon. J Oral Maxillofac Surg 1995 Jun;53(6):719-722; discusión 722. [Medline: 7776062]
- Chuong R, Piper MA. Fuga de líquido cefalorraquídeo asociada con la extracción del implante proplast de la articulación temporomandibular. Oral Surg Oral Med Oral Pathol 1992 Oct;74(4):422-425. [Medline: 1408012]
- Berarducci JP, Thompson DA, Scheffer RB. Perforación en la fosa craneal media como secuela del uso de un implante Proplast-Teflon para la reconstrucción de la articulación temporomandibular. J Oral Maxillofac Surg 1990 May;48(5):496-498. [Medline: 2329399]
- [Sin autores listados]. Recomendaciones para el manejo de pacientes con implantes de articulación temporomandibular. Taller de cirugía de implantes de articulación temporomandibular. J Oral Maxillofac Surg 1993 Oct;51(10):1164-1172. [Medline: 8410459]
- Herring S. Anatomía de la ATM y modelos animales. J Musculoskelet Neuronal Interact 2003 Dec;3(4):391-394; discusión 406 [Texto completo GRATIS] [Medline: 15758330]
- Angelo D, Morouço P, Alves N, Viana T, Santos F, González R. Elegir ovejas (Ovis aries) como modelo animal para la investigación de la articulación temporomandibular: caracterización morfológica, histológica y biomecánica del disco articular. Morphologie 2016 Jul:223-233 [Texto completo GRATIS] [doi: 10.1016/j.morpho.2016.06.002] [Medline: 27450042]
- Leiggener CS, Erni S, Gallo LM. Enfoque novedoso para el estudio de la cinemática de la mandíbula en una reconstrucción de ATM aloplástica. Int J Oral Maxillofac Surg 2012 Sep;41(9):1041-1045. [doi: 10.1016/j.ijom.2012.06.014] [Medline: 22819692]
- Little CB, Smith MM, Cake MA, Read RA, Murphy MJ, Barry FP. La iniciativa de histopatología OARSI - recomendaciones para evaluaciones histológicas de la osteoartritis en ovejas y cabras. Osteoarthritis Cartilage 2010 Oct;18 Suppl 3:S80-S92 [Texto completo GRATIS] [doi: 10.1016/j.joca.2010.04.016] [Medline: 20864026]
- Cake MA, Appleyard RC, Read RA, Smith MM, Murrell GA, Ghosh P. La ovariectomía altera las propiedades estructurales y biomecánicas del cartílago articular femoro-tibial ovino y aumenta el iNOS del cartílago. Osteoarthritis Cartilage 2005 Dec;13(12):1066-1075 [Texto completo GRATIS] [doi: 10.1016/j.joca.2005.07.001] [Medline: 16154775]
- Cohen W, Servais J, Polur I, Li Y, Xu L. Degeneración del cartílago articular en la articulación temporomandibular contralateral no quirúrgica en ratones con una discectomía parcial unilateral. J Oral Pathol Med 2014 Feb;43(2):162-165. [doi: 10.1111/jop.12113] [Medline: 24044578]
- Ahtiainen K, Mauno J, Ellä V, Hagström J, Lindqvist C, Miettinen S, et al. Células madre adiposas autólogas y discos de polilactida en la sustitución del disco de la articulación temporomandibular del conejo. J R Soc Interface 2013 Aug 06;10(85):20130287 [Texto completo GRATIS] [doi: 10.1098/rsif.2013.0287] [Medline: 23720535]
- Brown B, Chung W, Almarza A, Pavlick M, Reppas S, Ochs M. Enfoque inductivo, basado en andamiaje, de medicina regenerativa para la reconstrucción del disco de la articulación temporomandibular. J Oral Maxillofac Surg 2012 Nov;70(11):2656-2668. [doi: 10.1016/j.joms.2011.12.030]
- Xu L, Polur I, Lim C, Servais J, Dobeck J, Li Y, et al. Osteoartritis de inicio temprano de la articulación temporomandibular en ratones inducida por discectomía parcial. Osteoarthritis Cartilage 2009 Jul;17(7):917-922. [doi: 10.1016/j.joca.2009.01.002] [Medline: 19230720]
- Lai WT, Tsai Y, Su S, Su C, Stockstill JW, Burch JG. Análisis histológico de la regeneración de discos de la articulación temporomandibular en conejos utilizando una plantilla de colágeno reconstituido. Int J Oral Maxillofac Surg 2005 May;34(3):311-320. [doi: 10.1016/j.ijom.2004.05.003] [Medline: 15741041]
- Sato S, Goto S, Koeda S, Motegi K. Cambios en la red de fibras elásticas de la articulación temporomandibular del conejo tras la discectomía. J Oral Rehabil 2002 Sep;29(9):847-852. [Medline: 12366539]
- Sato S, Goto S, Motegi K. Cambios en la disposición de las fibras de colágeno de la articulación temporomandibular del conejo tras la discectomía. J Craniomaxillofac Surg 2002 Jun;30(3):178-183. [Medline: 12220997]
- Bjørnland T, Haanaes HR. Discectomía de la articulación temporomandibular: un estudio experimental en monos. J Craniomaxillofac Surg 1999 Apr;27(2):113-116. [Medline: 10342149]
- Ogi N, Kurita K, Ishimaru JI, Goss AN. Efecto a corto plazo del uso de un aloinjerto de disco congelado para la reparación de la articulación temporomandibular osteoartrítica en ovejas: un informe preliminar. J Oral Maxillofac Surg1999 Feb;57(2):139-144; discusión 144. [Medline: 9973121]
- Hinton R, Stinson J. Efecto de la dieta postoperatoria en la respuesta del cartílago condilar a la discectomía. J Oral Maxillofac Surg 1997 Nov;55(11):1259-1264. [Medline: 9371117]
