Un estudio clínico que mide aerosoles dentales con y sin un dispositivo HVE
Traducción automática
El artículo original está escrito en idioma EN (enlace para leerlo) .
Resumen
Introducción: Los dispositivos de extracción de alto volumen externos pueden ofrecer una forma de reducir cualquier partícula aerosol generada. El objetivo de este estudio fue medir el conteo de partículas durante los procedimientos dentales de aerosol y comparar los resultados con el uso de un dispositivo de extracción de alto volumen;
Métodos: Se llevó a cabo un estudio clínico comparativo que midió la cantidad de partículas aerosol PM1, PM2.5 y PM10 con y sin el uso de un dispositivo de extracción de alto volumen externo. En total, se monitorearon 10 procedimientos restaurativos con un contador de partículas industrial Trotec PC220. El muestreador de aire se colocó a la distancia de trabajo promedio de los clínicos involucrados en el estudio - 420 mm.;
Resultados: En el presente estudio, se registraron partículas aerosol a niveles estadísticamente significativos aumentados durante los procedimientos dentales sin un dispositivo de extracción de alto volumen externo en comparación con el uso del dispositivo. La hipótesis nula fue rechazada, ya que se encontraron diferencias significativas entre los resultados de la cantidad de conteo de partículas aerosol con y sin un dispositivo de extracción de alto volumen.;
Conclusión: Si los resultados del presente estudio se repiten en un entorno in vivo, un dispositivo de succión de alto volumen externo puede potencialmente reducir el riesgo de transmisión de partículas virales.
Introducción
Aerosoles y el virus Sars-Cov-2
A la luz de la pandemia de Sars-Cov-2, la Administración de Seguridad y Salud Ocupacional de los Estados Unidos ha clasificado los aerosoles producidos en odontología como una de las ocupaciones de muy alto riesgo para la transmisión de la enfermedad. Antes de investigar el presente estudio, debemos discutir cómo se generan los aerosoles y qué tamaño de partículas están presentes en cualquier aerosol potencial que se genere en un procedimiento dental para entender la importancia de reducir los aerosoles generados. Un aerosol es un sistema de dispersión que consiste en partículas sólidas y líquidas de varios tamaños que están suspendidas en un medio gaseoso. Al utilizar esta definición y los tres elementos importantes de los aerosoles, debemos considerar que es normal que un aerosol esté suspendido en el aire solo si tiene menos de 10 micrones de tamaño. Esto se debe a que a medida que estas gotas disminuyen de tamaño, también lo hace su masa relativa. Como tal, el impacto de la gravedad en estas partículas se reduce y pueden permanecer suspendidas en el aire durante mucho más tiempo.
El tamaño de las partículas que pueden estar potencialmente suspendidas en los aerosoles producidos puede variar de 0.001 a 100 micrones. Estas partículas se pueden definir según su tamaño: las partículas gruesas son de 2.5 a 10 micrones (clasificación PM10), las partículas finas son menores de 2.5 micrones (PM2.5) y las partículas ultrafinas son menores de 0.1 micrones (PM1). Para la transmisión humana de enfermedades, la dosis infecciosa requerida es pequeña. Los agentes virales y bacterianos tienen afinidad por componentes específicos de células y tejidos junto con factores patogénicos. La vía respiratoria oral-nasal puede canalizar partículas de aire de más de 10 micrones de tamaño. Esto representa un riesgo, ya que las partículas de menos de 10 micrones pueden ingresar al sistema respiratorio y las partículas más pequeñas de menos de 2.5 micrones pueden entrar en el saco alveolar. Las partículas ultrafinas, como la molécula del virus Sars-Cov-2, que son inferiores a 1 micrón, pueden potencialmente ingresar al sistema circulatorio a través de este mecanismo directamente o ser transportadas en una partícula más grande. El mecanismo de la respiración en los seres vivos también puede crear aerosoles en forma de bio-aerosoles. Estas gotas pueden producirse en grandes cantidades, por ejemplo, hasta tres mil en solo una tos. Las partículas de alta proyección también pueden generarse en mayor número (más de cuarenta mil) en la acción de estornudar.
Cómo se propagan las infecciones por vía aérea
Aún antes de que se descubrieran agentes infecciosos específicos como bacterias y virus, se reconoció el potencial de infección por la vía aérea, por ejemplo, la peste bubónica, también conocida como la 'peste negra', que se registró como propagada a través de una ruta aérea.
Esto se considera una preocupación en tiempos más recientes en los viajes aéreos. En un informe, el bacilo de micobacterium que causa tuberculosis se propagó a través de los pasajeros en un avión. Los pasajeros sentados más cerca de la fuente de la infección tenían más probabilidades de contraer la enfermedad.
Los mecanismos exactos por los cuales se propaga el virus sars-cov-2 siguen bajo investigación, pero la comprensión actual apunta a la transmisión a través de gotas aerosol. Por lo tanto, muchos gobiernos y autoridades de salud en todo el mundo han aconsejado a los profesionales dentales que procedan solo con procedimientos de emergencia y esenciales y eviten por completo los procedimientos dentales electivos.
Aerosoles Dentales
La acción mecánica de las herramientas utilizadas en la clínica dental puede producir partículas suspendidas como aerosoles, tales como el uso de piezas de mano dentales rápidas y lentas, escaladores ultrasónicos y jeringas de aire y agua. Estas herramientas utilizan aire de alta potencia o micromotores mecánicos de alta velocidad para funcionar, lo que puede crear estos aerosoles a través de la energía cinética que actúa en el proceso de instrumentación dental.
Dado que la boca contiene saliva, sangre y otras sustancias, los micro-organismos y partículas virales están siempre presentes. Los estudios han demostrado que la carga bacteriana alrededor de la boca del paciente durante un procedimiento de tratamiento oral es mayor en comparación con cuando no se les opera en un procedimiento dental. Las líneas de agua de la unidad dental son otra fuente potencial que contribuye a los micro-organismos transportados en la generación de aerosoles. Estas líneas de agua que suministran las piezas de mano y jeringas pueden contaminarse a través del uso, ya que el agua puede retroceder o por el agua entrante utilizada en la unidad del sillón dental. La pulverización de agua es generalmente la parte más visible del aerosol a simple vista, y es notada por el paciente y el personal dental.
Un estudio reciente examinó cómo la escalera ultrasónica puede transmitir aerosol particulado hasta seis pies y sin una corriente de aire, este particulado puede permanecer suspendido de 35 minutos a varias horas. Si el particulado suspendido es superior a 10 micrones, la gravedad puede hacer que estas partículas se asienten en las superficies circundantes, como el paciente y el área clínica inmediata, hasta dos metros. Durante estos procedimientos dentales, se sabe que varios equipos dentales, como las piezas de mano dentales, las jeringas de aire-agua, los escaladores ultrasónicos y las unidades de pulido por aire, producen unidades formadoras de colonias en comparación con los períodos pre y postoperatorios a través de estos bio-aerosoles generados.
¿Puede el salpicado de los procedimientos dentales propagar enfermedades?
Miller et al han concluido que los bio-aerosoles pueden contener millones de bacterias por pie cúbico de aire. King et al han afirmado que los aerosoles recuperados a seis pulgadas de un paciente, las unidades formadoras de colonias se redujeron sustancialmente a través de sistemas de reducción de aerosoles.
Durante un procedimiento dental convencional, se requiere que el paciente se siente con la boca abierta, exponiendo los fluidos que ocurren naturalmente, como la saliva y la sangre. Durante un procedimiento dental que utiliza escaladores ultrasónicos, la jeringa de aire/agua o dispositivos de turbina de aire de alta velocidad o micromotores, la acción mecánica puede esparcir estos fluidos corporales a través de salpicaduras fuera del sitio de operación hacia el entorno circundante. Es esta salpicadura la que puede tomar la forma de un aerosol de gotas de varios tamaños. Los constituyentes de estas gotas y su tamaño relativo han recibido los términos dentales 'salpicaduras' y 'aerosoles'. Las partículas más grandes que no están suspendidas pueden ser visibles donde ocurre la dispersión fuera del campo de operación, pero las partículas y gotas de menos de 50 micrones no son visibles a simple vista. Estas partículas más pequeñas tienen una masa mínima (menos de 10 micrones) y pueden permanecer en el aire durante minutos o incluso horas hasta que son inhaladas por los humanos. Una vez inhaladas, pueden viajar a los finos alvéolos pulmonares, potencialmente causando infecciones respiratorias.
Estos aerosoles y núcleos también pueden entrar en los sistemas de ventilación de la clínica dental y propagarse a otros sitios de operación.
Así, la posible propagación del virus sars-cov-2 en una clínica dental se caracteriza a través de tres vías: contacto directo con fluidos orales infectados, contacto directo con superficies contaminadas e inhalación de aerosoles particulados infecciosos.
El objetivo de este estudio fue medir el conteo de partículas durante los procedimientos de aerosol dental y comparar los resultados con los obtenidos cuando se utiliza un dispositivo de Extracción de Alto Volumen.
La hipótesis nula era que no se encontrarían diferencias en la cantidad de conteo de partículas de aerosol con o sin un dispositivo de Extracción de Alto Volumen.
Materiales y Métodos
Dispositivo muestreador de aire
En total, se monitorearon 5 procedimientos restaurativos diferentes con un contador de partículas industrial Trotec PC220. Este muestreador se envía con un certificado de calibración donde el muestreador está calibrado con un Filtro PC200/220 para Calibración Cero por el fabricante. Por lo tanto, el muestreador de aire no necesita calibrarse antes de su uso por el usuario. Este muestreador de aire cumple con la norma ISO 215014 - que se refiere específicamente a los Contadores de Partículas de Aerosoles por Dispersión de Luz - y es preciso dentro de +/- 95% con una pérdida de coincidencia de partículas del 5%. El muestreador se utilizó para medir el PM1 (partículas de tamaño 1 micrómetro (μm) o menos), PM2.5 (partículas de tamaño 1-2.5 micrómetros (μm)) y partículas de tamaño PM10 (partículas de tamaño 2.5-10 micrómetros (μm)) generadas en cada procedimiento. Los 5 procedimientos diferentes se llevaron a cabo tanto sin un dispositivo HVE en su lugar como repetidos por separado con el dispositivo HVE en su lugar para comparar el efecto del HVE en los conteos de partículas registrados. El muestreador de aire utiliza detección por dispersión láser de múltiples ángulos. La luz dispersada se recogerá en un ángulo especificado y, de acuerdo con la intensidad de la dispersión, se pueden obtener diámetros de partículas equivalentes y el número de materia particulada suspendida de diferentes tamaños por unidad de volumen.
Distancia de Trabajo
Para cada procedimiento, el muestreador de aire se colocó a la distancia de trabajo promedio registrada de los clínicos involucrados en el estudio - 420 mm. Es decir, se midió la distancia de trabajo de cada uno de los dentistas y luego se utilizó este promedio para colocar el muestreador de aire en una unidad a la misma distancia del modelo y, por lo tanto, de la fuente del aerosol. Específicamente y espacialmente, el muestreador se colocó a 420 mm directamente a la derecha de la unidad de cabeza fantasma en una unidad dental adyacente. Para los propósitos del presente estudio, no se tomaron medidas a distancias más cercanas o más lejanas de la fuente del aerosol. El muestreador de aire fue pegado alrededor de los sellos y juntas para prevenir la contaminación de la unidad y proporcionar una superficie limpiable entre mediciones.
Extracción de Alto Volumen
La unidad utilizada en este estudio fue una Vacstation de Eighteeth. La VacStation utiliza un sistema de filtración de múltiples niveles (HEPA, filtro de algodón de alta fibra, carbón activado, KMnO4, filtro de ceramsita, 2º HEPA 13) y luz UV C. La Vacstation se colocó con el orificio de succión circular a 300 mm frente a la cabeza fantasma. Esta posición estaría - en un entorno in vivo - posicionada sobre el pecho del paciente y frente a su boca. La Vacstation se encendió en la configuración de succión máxima. La Vacstation es capaz de variar la configuración de succión, pero para los propósitos del presente estudio, la configuración se dejó en máxima para un efecto repetible.
Configuración del estudio
Los voluntarios para el estudio fueron cuatro dentistas que trabajaban en una sola clínica dental utilizando la misma unidad de silla. Para evitar que factores externos afectaran los resultados, se mantuvo la presión de la habitación en el mismo nivel con las ventanas cerradas, sin aire acondicionado y sin purificador de aire en funcionamiento.
El muestreo se realizó en un modelo de cabeza fantasma en una silla dental en la posición de un paciente. La ventilación de la habitación se apagó y las ventanas se cerraron. Todas las unidades tenían la funcionalidad normal del equipo en funcionamiento (por ejemplo, refrigeración por agua, eyector de saliva estándar) como se utiliza en la silla para la práctica normal.
El día del estudio, se instruyó a los dentistas voluntarios a realizar tratamientos restaurativos normales en el modelo como se describe a continuación.
El período de muestreo para el componente del estudio sin el uso de un extractor de alto volumen se registró desde el inicio de ese procedimiento específico. La duración del procedimiento fue de uso continuo durante 1 minuto. La medición de muestreo continuó durante un minuto o hasta que los niveles de partículas en el aire regresaran a niveles normales.
Procedimientos probados
- Jeringa de aire/agua tres en uno (mezcla de aire y agua); La jeringa de aire/agua tres en uno fue dirigida hacia la región anterior inferior con succión normal del aspirador recolectando el agua producida.
- Micromotor de alta velocidad con agua; Se utilizó el micromotor de alta velocidad para perforar un diente anterior inferior en el modelo dental como cavidades mesiales. En el segundo procedimiento con el dispositivo HVE en su lugar, se perforó el mismo diente en la superficie distal.
- Contraángulo de alta velocidad con agua; Se utilizó el contraángulo de alta velocidad para perforar un diente anterior inferior en el modelo dental como cavidades mesiales. En el segundo procedimiento con el dispositivo HVE en su lugar, se perforó el mismo diente en la superficie distal.
- Contraángulo de baja velocidad con agua; Se utilizó el contraángulo de baja velocidad para perforar un diente anterior inferior en el modelo dental como cavidades mesiales. En el segundo procedimiento con el dispositivo HVE en su lugar, se perforó el mismo diente en la superficie distal.
- Escalado ultrasónico con agua; Se utilizó el escalador ultrasónico para escalar alrededor de los márgenes gingivales de los dientes anteriores inferiores en el modelo.
Validación y nivel de antecedentes
El muestreador de aire se utilizó para medir la misma habitación durante una hora antes y después de que terminaran los procedimientos para analizar que no hubo fluctuación natural de partículas en el aire. Rango:
- PM1 3-6 µg/m3,
- PM2.5 6-8 µg/m3,
- PM10 7-10 µg/m3 de partículas.
Aprobación Ética
El muestreo se realizó utilizando rutinas diarias y cumplió con las medidas de protección actuales contra el sars-cov-2, pero no involucró intervención en sujetos humanos. No se registraron datos personales de los participantes y, por lo tanto, no hubo requisito de aprobación ética.
Análisis Estadístico
Los datos capturados por el contador de partículas se tabularon en una hoja de cálculo de Excel para Mac 2016 y se analizaron en SPSS 26 de IBM. Se realizaron comparaciones utilizando un análisis de varianza de un solo factor (ANOVA) para grupos independientes, con un nivel de significancia de Tukey de 0.05, de múltiples comparaciones utilizando SPSS 26 de IBM (una comparación de medias para cada procedimiento con y sin el dispositivo de extracción de alto volumen externo) se utilizó para determinar la significancia de cada una de las medias. El nivel de significancia se estableció en P < 0.05 para todos los análisis.
Resultados
Los resultados se muestran para el período de medición de cada conteo de partículas, PM1, PM2.5 y PM10. En las Figuras 1 y 2, los datos se presentan como un gráfico del conteo de partículas medido para cada tamaño de partícula durante el procedimiento durante un minuto y durante un minuto después del procedimiento.
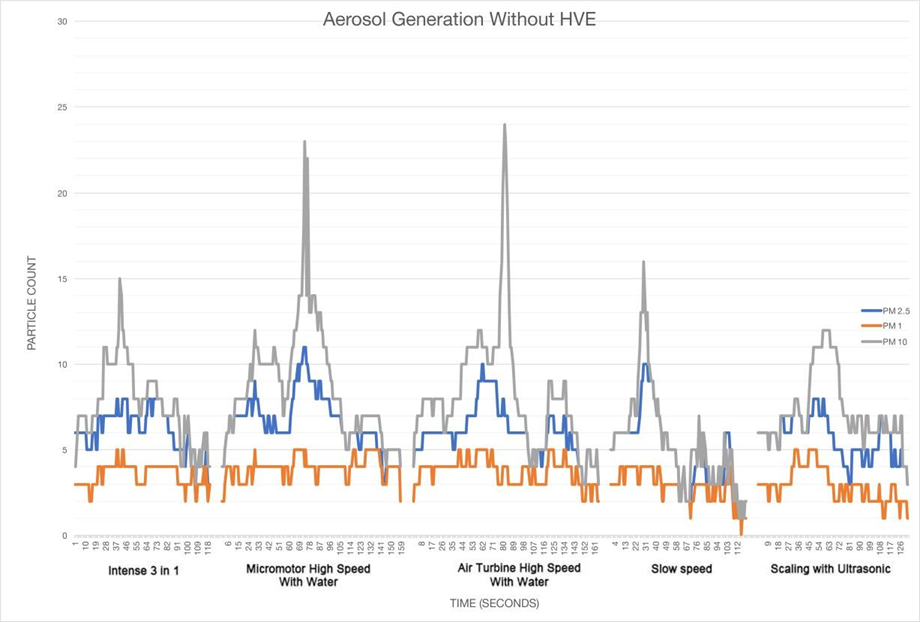
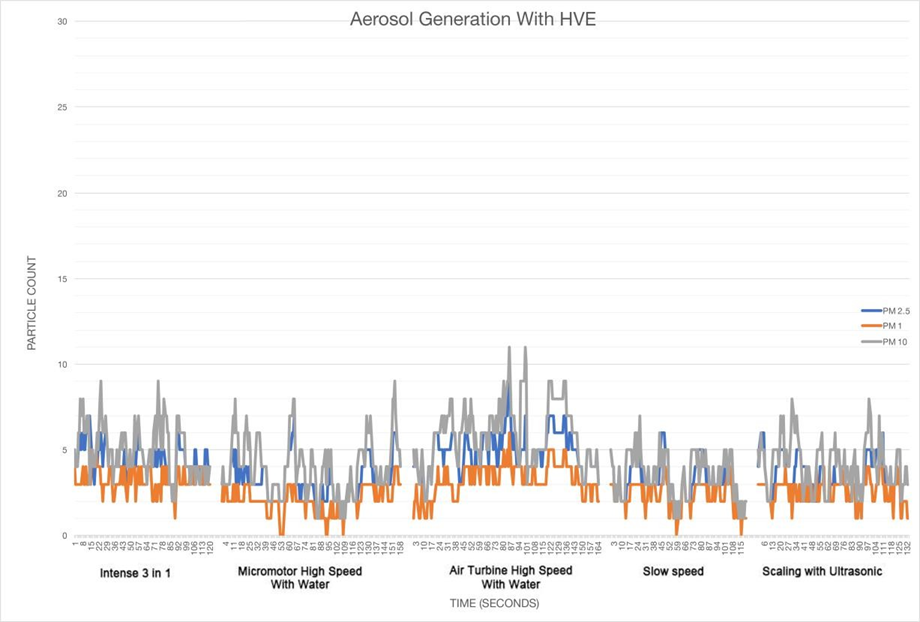
En el presente estudio, hay una clara diferencia entre los resultados como se muestra en los dos gráficos que exhiben los datos registrados a lo largo del tiempo.
Las Tablas 1, 2 y 3 muestran el conteo máximo de partículas registrado durante cada procedimiento;


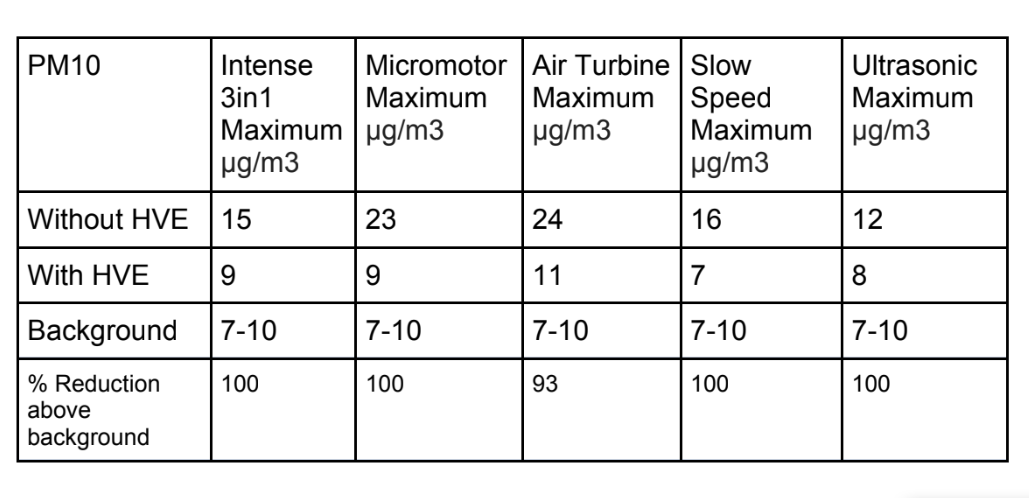
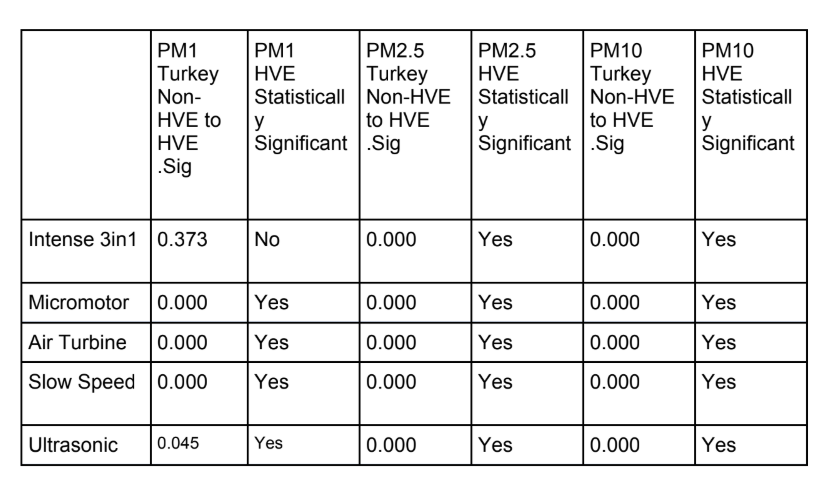
Podemos ver a partir del análisis estadístico en SPSS 26 que con una comparación de medias de Tukey (Tabla 4) hay una diferencia estadísticamente significativa en las muestras de datos registradas para cada procedimiento dental cuando se utiliza un dispositivo de extracción de alto volumen externo. La única excepción a esto es el conteo de partículas PM1 en un procedimiento 3 en 1.
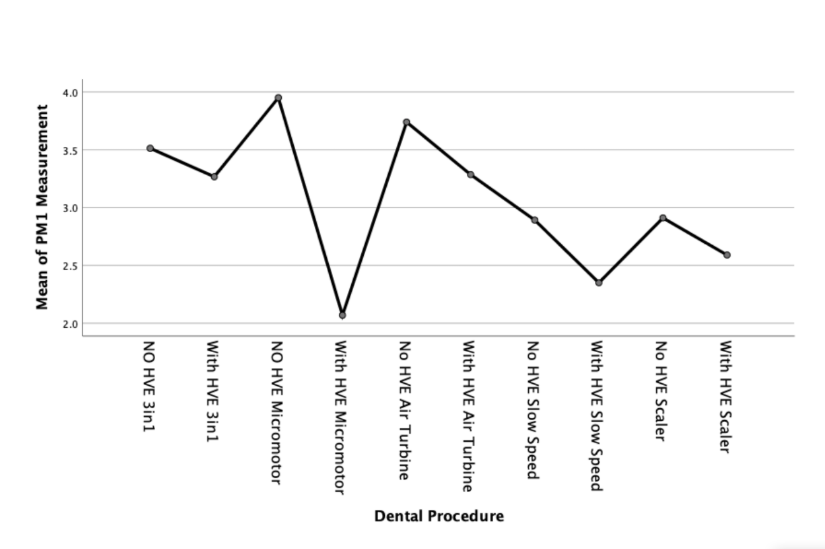
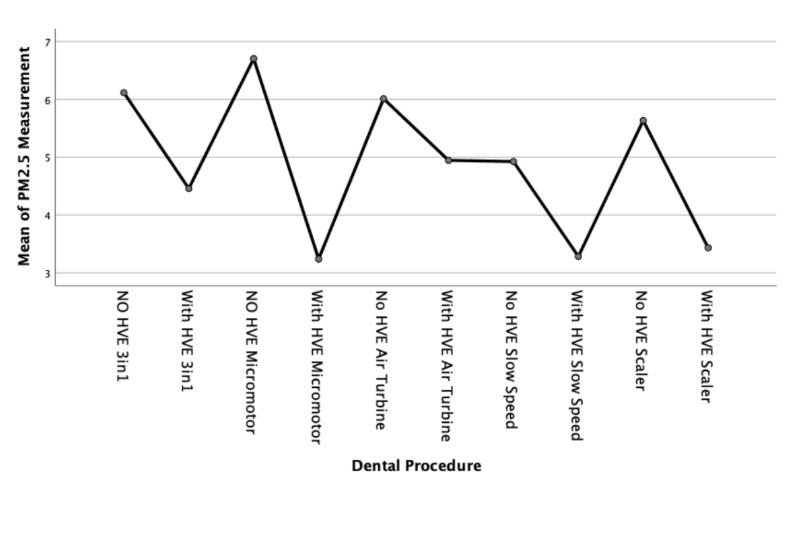
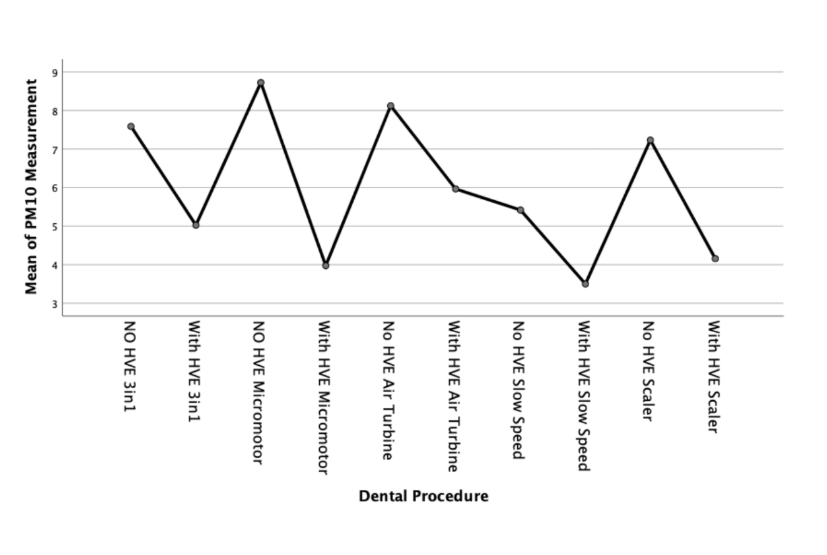
Podemos examinar más a fondo esta diferencia con un gráfico de medias para cada tamaño de partícula, como se muestra en las Figuras 3, 4 y 5;
Discusión
Se rechazó la hipótesis nula, ya que se encontraron diferencias significativas entre los resultados de la cantidad de recuento de partículas de aerosol con y sin un dispositivo de Extracción de Alto Volumen. El propósito del presente estudio fue medir el recuento de partículas durante los procedimientos de aerosol dental y comparar los resultados con cuando se utiliza un dispositivo de Extracción de Alto Volumen. La razón por la cual esto es de particular importancia en la práctica dental actual es el riesgo de transmisión del virus SARS-CoV-2 a través de partículas aerosol.
Diámetro viral del SARS-CoV-2 y relevancia para el tamaño de las partículas.
Zhu et al han discutido "Los micrografías electrónicas de partículas de 2019-nCoV teñidas negativamente eran generalmente esféricas con algo de pleomorfismo. El diámetro variaba de aproximadamente 60 a 140 nm." Usando este diámetro y asumiendo que el virus es una esfera[36], podemos asumir que dado que el virus es aproximadamente una milésima de las partículas de aerosol en este estudio, cualquier partícula de aerosol de tamaño PM1, PM2.5 o PM10 producida puede llevar el virus y, por lo tanto, potencialmente transmitir la enfermedad si se inhala.
Tamaños de aerosol
Partículas de tamaño PM1 generadas;
En el presente estudio, las partículas de tamaño PM1 generadas con todos los procedimientos parecen permanecer dentro del rango muestreado en las mediciones de control sin que se realice ningún procedimiento. Sin embargo, fuera del procedimiento 3 en 1, hubo una reducción estadísticamente significativa en el conteo de partículas cuando se utilizó un dispositivo de extracción de alto volumen externo.
Partículas de tamaño PM2.5 generadas;
Hubo un claro aumento en las partículas PM2.5 generadas durante los procedimientos dentales. Este aumento estadísticamente significativo fue aproximadamente el doble de las mediciones de muestra de fondo normales. Con el uso de un dispositivo de extracción de alto volumen HVE externo, las muestras tomadas durante los cinco procedimientos dentales se redujeron estadísticamente de manera significativa. Hubo un ligero aumento en los niveles medidos hacia el final del procedimiento de turbina de aire, pero esto fue estadísticamente insignificante (11 µg/m3 con HVE frente a 24 µg/m3 sin HVE).
Partículas de tamaño PM10 generadas;
Las partículas de tamaño PM10 generadas en cada uno de los procedimientos siguieron un patrón similar, aunque amplificado, al de las partículas de tamaño PM2.5 generadas. Los niveles máximos de partículas generadas fueron aproximadamente tres veces los niveles de fondo de PM10. Con el uso de un dispositivo de extracción de alto volumen externo HVE, las muestras tomadas durante los cinco procedimientos dentales se redujeron estadísticamente de manera significativa.
Interpretación
Por lo tanto, podemos interpretar estos resultados como que no se generan partículas PM1, o muy pocas, durante los procedimientos dentales 3en1, ya que la diferencia no fue estadísticamente significativa.
Hay un aumento estadísticamente significativo de entre dos y tres veces los niveles de fondo de µg/m3 de partículas de tamaño PM2.5 y PM10 en comparación con los resultados registrados durante procedimientos dentales sin el uso de un HVE externo.
Relevancia Biológica
Una limitación en la interpretación de estos resultados es la relevancia biológica con respecto al virus SARS-CoV-2. Este virus es nuevo y la infectividad relativa y los mecanismos de transmisión están actualmente bajo investigación.
En el brote de SARS en 2003, Kan et al. estudiaron la relación entre los niveles de partículas y la mortalidad. El estudio mostró que las PM con un diámetro aerodinámico de 10 m (PM10) estaban asociadas positivamente con la mortalidad por SARS.
También se ha informado que los aerosoles asociados con patógenos altamente virulentos como el SARS podrían viajar más de dos metros. Aunque no son de origen dental, Feng et al. realizaron un análisis ecológico que encontró una relación positiva entre el conteo de partículas PM2.5 y la transmisión viral en Beijing.
Los aerosoles pequeños tienen más potencial para ser inhalados profundamente en los pulmones, lo que puede causar potencialmente infección en los tejidos alveolares de las vías respiratorias inferiores. Recientes trabajos de investigación se han centrado en proporcionar una mejor comprensión sobre la transmisión de aerosoles y gotas, lo que ha proporcionado evidencia de que los aerosoles pueden desempeñar un papel importante en la transmisión del virus SARS-CoV-2. Duguid et al. estudiaron el número de gotas y aerosoles generados de tamaños de 1 a 100 μm y encontraron que la tos y los estornudos producían desde unas pocas hasta unos pocos cientos de gotas y aerosoles por metro cúbico. Sin embargo, persiste la controversia entre muchos investigadores sobre los modos de transmisión a través de gotas o aerosoles y el riesgo cuantificable asociado con los niveles de cualquiera de ellos.
En el presente estudio, se registraron niveles de partículas en aerosol estadísticamente significativos aumentados durante los procedimientos dentales sin un dispositivo de extracción de alto volumen externo en comparación con el dispositivo. Estos niveles aumentados fueron de alrededor de dos docenas de μm por metro cúbico.
Minimizar aerosoles y salpicaduras
Estudios recientes han demostrado que el virus SARS-CoV-2 puede transmitirse a través de partículas en el aire. Históricamente, estudios anteriores han mostrado que hay una correlación positiva entre PM2.5 y tamaños de partículas más grandes, y la transmisión de virus como la influenza. Los Centros para el Control y la Prevención de Enfermedades (CDC) llevaron a cabo un estudio que mostró que el virus Sars-CoV-2 pudo permanecer viable durante hasta 72 horas en algunas superficies.
Se podría argumentar que el riesgo de transmisión en el entorno dental a través de aerosoles es menor, ya que las gotas de aerosol pueden ser completamente de la línea de agua. Sin embargo, cuando observamos un estudio sobre salpicaduras y aerosoles generados por un escalador ultrasónico sin agua de refrigeración utilizada in vitro, todavía había una cantidad sustancial de aerosol y salpicaduras formadas a partir de pequeñas cantidades de líquido colocadas en el sitio de operación para simular sangre y saliva. Por lo tanto, debemos buscar formas de mitigar este riesgo durante la actual crisis de sars-cov-2.
Harrel et al escribieron que “ningún enfoque o dispositivo único puede minimizar completamente el riesgo de infección para el personal dental y otros pacientes. Un solo paso reducirá el riesgo de infección en cierta medida, otro paso añadido al primer paso reducirá el riesgo restante, hasta que el riesgo sea mínimo.” Este es un enfoque sensato para proporcionar protección en capas para la mitigación del riesgo. Harrel también discute que en la reducción de aerosoles dentales, la primera capa de defensa son las barreras de protección personal, como mascarillas, guantes, viseras, gafas de seguridad y redes para el cabello. La segunda capa de defensa es el uso rutinario de un enjuague antiséptico preprocedimental con un enjuague bucal como peroxilo/yodopovidona o clorhexidina. La tercera capa de defensa es el uso regular de un evacuador de alto volumen (HVE) ya sea por un asistente o conectado al instrumento que se está utilizando. Una capa adicional de defensa también podría ser el empleo de una herramienta para reducir la contaminación por aerosoles que escapan del área de operación, como un filtro HEPA. Estas capas adicionales de defensa se encuentran comúnmente o se pueden implementar fácilmente en la mayoría de las prácticas dentales.
También se ha recomendado que las prácticas dentales instalen flujo de aire a presión negativa para prevenir la transmisión aérea a través de aerosoles. Algunos, incluidos Harrel et al, han sugerido que el uso de un enjuague bucal de 0.2% de Clorhexidina o Listerine preoperatoriamente podría ser beneficioso, ya que se ha demostrado que reducen la carga bacteriana oral en aerosoles, pero no hay estudios revisados por pares de alta calidad sobre la actividad virucida del Peróxido de Hidrógeno. Se ha hipotetizado que el yodo tiene un mayor valor para este propósito que la clorhexidina.
La succión de alto volumen correctamente colocada y el evacuador cerca de la pieza de mano y la boca pueden reducir el 90% de la salida de aerosol. Durante las prácticas conservadoras, se piensa que el uso de la barrera de dique de goma también reduce el riesgo significativamente hasta un 98.5%. Los resultados del presente estudio confirman estas cifras, al mismo tiempo que benefician al cirujano, ya que la unidad de extracción de alto volumen extraoral no requiere un asistente para mantener la posición.
Para prevenir el riesgo de transmisión, especialmente durante la pandemia de sars-cov-2, se ha aconsejado en todo el mundo el uso de equipo de protección personal de alto riesgo en diferentes grados. En el Reino Unido también ha habido un aviso sobre un tiempo de inactividad después de los procedimientos que generan aerosoles. Tanto el equipo de protección como el período de inactividad son un gran cambio con respecto a la norma clínica y podrían afectar la sostenibilidad y el funcionamiento de las clínicas dentales. Reducir la necesidad de apartarse de la norma podría mejorar el acceso de los pacientes a través de la reducción de los tiempos de espera después del procedimiento y mejorar la comodidad para el operador.
Conclusiones
En el momento de completar el presente estudio, no ha habido estudios que comparen el uso de dispositivos de extracción de alto volumen externos en odontología.
El propósito del presente estudio fue medir el conteo de partículas durante los procedimientos de aerosol dental y comparar los resultados con cuando se utiliza un dispositivo de extracción de alto volumen, y los resultados muestran una potencial utilidad clínica para reducir y mitigar algunos riesgos de transmisión del virus SARS-CoV-2.
Los aerosoles y salpicaduras generados durante los procedimientos dentales tienen el potencial de propagar infecciones al personal dental y a las personas dentro de la consulta dental. Si bien, como con todos los procedimientos de control de infecciones, es imposible eliminar completamente el riesgo que representan los aerosoles dentales, es importante minimizar estos riesgos tanto como sea posible. Los resultados del presente estudio muestran que un dispositivo de extracción de alto volumen externo puede reducir el conteo de partículas de aerosol durante los procedimientos dentales.
Aunque los resultados de este estudio específico no muestran un vínculo directo entre la concentración aumentada de partículas PM1, PM2.5 o PM10 generadas por procedimientos dentales, hemos demostrado que hay una concentración estadísticamente significativa aumentada de partículas PM2.5 y PM10 durante cada uno de los cinco procedimientos sin el uso de un dispositivo HVE externo. Por lo tanto, podemos interpretar estos resultados que si el virus SARS-CoV-2 puede estar presente en gotas de aerosol y partículas, existe un riesgo potencialmente aumentado de transmisión de SARS-CoV-2 a partir de procedimientos que generan aerosoles y que producen concentraciones aumentadas de estos tamaños de partículas. Sin embargo, si estudios adicionales muestran que las partículas de aerosol se producen en un entorno clínico in vivo, puede ser posible reducir y mitigar efectivamente el riesgo asociado con el uso de dispositivos de extracción HVE externos.
Se sugieren una serie de limitaciones en nuestro estudio in vitro, a saber, los efectos in vivo como la saliva, la sangre, la respiración, la tos, la interacción con el paciente, etc., que deben tenerse en cuenta y pueden impactar los resultados en un entorno de paciente in vivo.
Por lo tanto, se propone que se requiere un estudio adicional ampliado para evaluar el impacto de la duración aumentada de la generación de aerosoles, así como el efecto acumulativo de otros factores de mitigación de riesgos, como el dique de goma, purificadores de aire, aumento del flujo de aire por apertura de ventanas, etc. También se prevé que en este estudio ampliado podamos comparar estos resultados con eventos expiratorios como la tos o el estornudo directamente.
Otra limitación fue el uso de solo un tipo de dispositivo de extracción de alto volumen externo. Estos dispositivos son nuevos y no son económicos. Un estudio adicional debería comparar varios tipos y marcas para investigar su capacidad relativa para reducir el recuento de partículas de aerosol en un entorno clínico in vivo.
Autores: Adam Nulty, Chris Lefkaditis, Patrik Zachrisson, Quintus Van Tonder y Riaz Yar
Referencias:
- Departamento de Trabajo de los Estados Unidos Administración de Seguridad y Salud Ocupacional. COVID-19 - Control y Prevención / Trabajadores y Empleadores de Odontología. Marzo 2020 [Internet] Accedido el 14 de junio de 2020; Disponible en: https://www.osha.gov/SLTC/covid-19/dentistry.html]
- An N, Yue L, Zhao B. Zhonghua Kou Qiang Yi Xue Za Zhi. Cognición de gotas y aerosoles en clínicas orales y medidas de prevención y control de infecciones. Revista China de Estomatología. 220; 55(4):223-228.
- Zemouri C, Volgenant CMC, Buijs MJ, et al. Aerosoles dentales: composición microbiana y distribución espacial. J Oral Microbiol. 2020; 12(1):1762040.
- Wurie F. Características de la producción de partículas exhaladas en voluntarios sanos: posibles implicaciones para enfermedades infecciosas. F1000 Res 2013; 2: 14.
- Tang JW, Li Y, Eames I, Chan PKS, Ridgway GL. Factores involucrados en la transmisión de aerosol de infecciones y control de ventilación en instalaciones de atención médica. 2006; 64(2).
- Eugen C, Carl E, Cook MS. Caracterización de aerosoles infecciosos en instalaciones de atención médica: una ayuda para controles de ingeniería efectivos y estrategias preventivas. Revista Americana de Control de Infecciones. 1998; 26(4).
- Froum S. COVID-19 y el problema con los aerosoles dentales, en Perio-Implant Advisory. 2020; 7 de abril
- Acharya S, Priya H, Purohit B, Bhatt M. Contaminación por aerosol en una clínica dental universitaria rural en el sur de India. Int J Infect Control. 2010; 6:1-7.
- Hallier C, Williams D, Potts A. 2010 Un estudio piloto de reducción de bioaerosoles utilizando un sistema de limpieza de aire durante procedimientos dentales. British Dental Journal, 2010.
- Wiley J. 1987. La vía aerobiológica de microorganismos.
- Kenyon TA, Valway SE, Ihle WW, Onorato IM, Castro KG. Transmisión de Mycobacterium tuberculosis resistente a múltiples fármacos durante un largo vuelo en avión. N Engl J Med. 1996; 334(15):933-8.
- Yet L. Análisis aerodinámico de SARS-CoV-2 en dos hospitales de Wuhan. Nature. 2020
- Chan J, Wet F. Un brote familiar de neumonía asociado con el nuevo coronavirus 2019 que indica transmisión de persona a persona: un estudio de un brote familiar. Lancet. 2020; 395,514-523
- Huang C. Características clínicas de pacientes infectados con el nuevo coronavirus 2019 en Wuhan, China. Lancet. 2020; 395,497-506
- CDC. Precauciones interinas de control de infecciones domésticas para procedimientos que generan aerosoles en pacientes con síndrome respiratorio agudo severo (SARS). Disponible en: “www.cdc.gov/ncidod/sars/ aerosolinfectioncontrol.htm”. Accedido: 11 de junio de 2020.
- Asociación Dental Americana. Síndrome respiratorio agudo severo (SARS). Disponible en “www.ada.org/prof/resources/topics/sars.asp”. Accedido: 10 de junio de 2020.
- Leggat PA. Aerosoles bacterianos en la clínica dental: una revisión. Int Dent J., 2001; 51(1).
- Freeman J. Riesgo de contaminación por aerosol alrededor de la silla dental. Dental Nursing. 2013; 9(1).
- Bentley CD, Burkhart NW, Crawford JJ. Evaluación de la contaminación por salpicaduras y aerosoles durante procedimientos dentales. JADA. 1994; 125: 579-84.
- Volgenant CMC, de Soet JJ, Transmisión cruzada en la oficina dental: ¿Esto te enferma?. Current Oral Health Reports, 2018.
- Gross KB, Overman PR, Cobb C, Brockmann S. Generación de aerosol por dos escaladores ultrasónicos y un escalador sónico: un estudio comparativo. J Dent Hyg 1992; 66:314-8.
- Miller RL. Características de aerosoles que contienen sangre generados por instrumentos dentales eléctricos comunes. Am Ind Hyg Assoc J. 1995; 56(7):670-676.
- Sawhney A, Venugopal S, Babu GR, et al. Aerosoles cuán peligrosos son en la práctica clínica. J Clin Diagn Res. 2015; 9(4):ZC52-ZC57.
- Bentley CD, Burkhart NW, Crawford JJ. Evaluación de la contaminación por salpicaduras y aerosoles durante procedimientos dentales. J Am Dent Assoc 1994; 125:579-84.
- Williams GH 3rd, Pollok NL 3rd, Shay DE, Barr CE. Purga de aire laminar de microorganismos en aerosoles dentales: procedimientos profilácticos con el escalador ultrasónico. J Dent Res. 1970; 49:1498.
- Miller RL, Micik RE, Abel C, Ryge G. Estudios sobre aerobiología dental: II. Salpicaduras microbianas expulsadas de la cavidad oral de pacientes dentales. J Dent Res 1971; 50:621-5
- Miller RL. Generación de infección aérea por equipos dentales de alta velocidad. J Am Soc Prev Dent 1976; 6:14- 7.
- King TB, Muzzin KB, Berry CW, Anders LM. La efectividad de un dispositivo de reducción de aerosol para escaladores ultrasónicos. J Periodontol 1997; 68:45-9.
- Harrel SK. 2004. Propagación aérea de enfermedades - las implicaciones para la odontología. Journal of the California Dental Association, 2004; 32(11):901-906
- Harrel SK, Molinari J. Aerosoles y salpicaduras en odontología: una breve revisión de la literatura y las implicaciones del control de infecciones. Journal of the American Dental Association. 2004
- Micik RE, Miller RL, Mazzarella MA, Ryge G. Estudios de aerobiología: aerosoles bacterianos generados durante procedimientos dentales. J Dent Res. 1968; 48 : 49- 56.
- van Doremalen N, Bushmaker T, Morris DH, et al. Estabilidad de aerosol y superficie de SARS-CoV-2 en comparación con SARS-CoV-1. N Engl J Med. 2020; 382(16):1564-1567.
- Centros para el Control y la Prevención de Enfermedades. Directrices para el control de infecciones en entornos de atención dental – Informe Semanal de Morbilidad y Mortalidad. 19 de diciembre de 2003/52(RR17);1-61. Directrices del CDC para el Control de Infecciones. Atlanta: Centros para el Control y la Prevención de Enfermedades.
- Abel LC, Miller RL, Micik RE, Ryge G. Estudios sobre aerobiología dental. IV. Contaminación bacteriana del agua suministrada por unidades dentales. J Dent Res. 1971; 50(6):1567-1569.
- Informe científico de la OMS 27 de marzo de 2020 Disponible en: https://www.who.int/publications-detail/modes-of- transmission-of-virus-causing-covid-19-implications-for-ipc-precaution-recommendations
- Zhu N, Zhang D, Wang W, Li X, Yang B, Song J, Zhao X, Huang B, Shi W, Lu R, Niu P, Zhan F, Ma X, Wang D, Xu W, Wu G, Gao GF, Tan W. Equipo de Investigación y Investigación del Nuevo Coronavirus de China Un nuevo coronavirus de pacientes con neumonía en China. New England Journal of Medicine. 2020; 382:727–733
- Kan HD, Chen BH, Fu CW, Yu SZ, Mu LN. 2005. Relación entre la contaminación del aire ambiente y la mortalidad diaria de SARS en Beijing. Biomed Environ Sci 18(1):1-4.
- Kutter JS, Spronken MI, Fraaij PL, Fouchier RA, Herfst S. 2018. Rutas de transmisión de virus respiratorios entre humanos. Current Opinion in Virology 28:142-151.
- Feng C, Li J, Sun W, Zhang Y, Wang Q. 2016. Impacto de la exposición a material particulado fino (PM2.5) en el riesgo de enfermedad similar a la influenza: un análisis de series temporales en Beijing, China. Environ Health 15:17.
- Thomas RJ. Tamaño de partícula y patogenicidad en el tracto respiratorio. Virulence. 2013;4:847–858.
- Morawska L, Cao J. Transmisión aérea de SARS-CoV-2: el mundo debería enfrentar la realidad. Environ. Int. 2020;105730
- Wang J, Du G. COVID-19 puede transmitirse a través de aerosol. Ir. J. Med. Sci. 2020:1–2.
- Duguid JP. Los números y los sitios de origen de las gotas expulsadas durante actividades expiratorias. Edinb. Med. J. 1945;52:385–401
- Zhen-Dong G et al. Distribución de aerosol y superficie del coronavirus del síndrome respiratorio agudo severo 2 en salas de hospital, Wuhan, China. Revista de Enfermedades Infecciosas Emergentes. 2020; 26
- Su W et al. Los efectos a corto plazo de los contaminantes del aire en enfermedades similares a la influenza en Jinan, China. BMC Public Health. 2019; 19,1319.
- Barnes JB, Harrel SK, Rivera-Hidalgo F. Contaminación por sangre de los aerosoles producidos por el uso in vivo de escaladores ultrasónicos. J Periodontal 1998; 69:434-8.
- Recomendaciones de control de infecciones para la oficina dental y el laboratorio dental. Consejo de Asuntos Científicos de la ADA y Consejo de Práctica Dental de la ADA. JADA, 1996; 127:672-80.
- Pippen DJ, Verderame RA, Weber KK. Eficacia de las mascarillas en la prevención de la inhalación de contaminantes en el aire. J Oral Maxillofac Surg. 1987; 45:319-23.
- Logothetis DD, Martinez-Welles JM. Reducción de la contaminación bacteriana por aerosol con un enjuague previo de gluconato de clorhexidina. JADA. 1995; 126: 1634-9.
- Harrel SK, Barnes JB, Rivera-Hidalgo F. Reducción de aerosoles producidos por escaladores ultrasónicos. J Periodontol. 1996; 67(1):28-32.
- Klyn SL, Cummings DE, Richardson BW, Davis RD. Reducción de la pulverización que contiene bacterias producida durante el escalado ultrasónico. Gen Dent 2001; 49(6):648-52.
- Kampf G, Todt D, Pfaender S, Steinmann E. Persistencia de los coronavirus en superficies inanimadas y su inactivación con agentes biocidas [la corrección publicada aparece en. J Hosp Infect. 2020; 104(3):246-251.
- Jacks ME. Una comparación de laboratorio de dispositivos de evacuación en la reducción de aerosoles. J Dent Hyg. 2002; 76(3):202- 6.
- Cochran MA, Miller CH, Sheldrake MA. La eficacia del dique de goma como barrera para la propagación de microorganismos durante el tratamiento dental. JADA. 1989; 199: 141-4.
- OCDO. Procedimiento operativo estándar - Transición a la recuperación 2020 [Accedido el 10 de junio] Disponible en: https://www.england.nhs.uk/coronavirus/wp-content/uploads/sites/52/2020/06/C0575-dental-transition- to-recovery-SOP-4June.pdf]
